1��ѡ���� ijͬѧ����ͼ��ʾ��װ�ý��е��ʵ�飮����˵����ȷ���ǣ�������
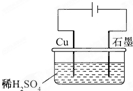
A���������У�ͭ�缫����H2����
B�������ڣ�����Ӧ����ʽΪ��Cu+H2SO4
CuSO4+H2��
C�����һ��ʱ���ʯī�缫����ͭ����
D�������������У�H+��Ũ�Ȳ�������
�ο��𰸣�A��ͭ�缫�͵�Դ��������������������ͭʧ���ӷ���������Ӧ���缫 ��ӦCu-2e-=Cu2+��ͭ�缫���������ɣ���A����
B�����ԭ��������ͭʧ��������ͭ���ӣ�������Һ���������������õ��������������������ڣ�����Ӧ����ʽΪ��Cu+H2SO4���.CuSO4+H2������B��ȷ��
C�����������������������������ɵ�ͭ���ӻ���������������ͭ���������Դ��������ӣ������������õ���������ͭ����C��ȷ��
D�����Ե缫��Ȼ��������H+�������ŵ磬���H2�ų�..H+����٣���D����
��ѡBC��
���������
�����Ѷȣ�һ��
2��ѡ���� ��14�֣������ܡ�����δ�������������Դ��
�� ��25��,101KPa�����£�1 g������ȫȼ������Һ̬ˮʱ�ų�142.9kJ���������ʾ����ȼ���ȵ��Ȼ�ѧ����ʽΪ ��
�� ����ͨ��������ˮú���ķ����Ƶá�����CO(g)+ H2O(g) CO2(g)+H2(g) ��H��0����850��ʱ��ƽ�ⳣ��K=1��
CO2(g)+H2(g) ��H��0����850��ʱ��ƽ�ⳣ��K=1��
(1)�������¶���950�棬�ﵽ��ƽ��״̬ʱK ���������������������1��
(2)850��ʱ������һ�ݻ��ɱ���ܱ�������ͬʱ����1.0 molCO��3.0mol H2O��1.0 molCO2��x mol H2����
�ٵ�x = 5.0ʱ������ƽ���� �������Ӧ�����淴Ӧ����������С�
����Ҫʹ������Ӧ��ʼʱ������Ӧ������У���xӦ����������� ��
������x="5.0" mol��x="6.0" mol���������ʵ�Ͷ�ϲ��䣬��������Ӧ�ﵽƽ����H2����������ֱ�Ϊa%��b%����a ���������������������b��
�� ��ˮ������õ�ˮ�Ĺ���Ҳ���Բ������������������õ�������������ˮ��õ�ˮ��ԭ��ͼ����֪��ˮ�к�Na����Cl����Ca2����Mg2����SO42�������ӣ��缫Ϊ���Ե缫��������������⣺

(1)�����ӽ���Ĥ��ָ______________ (��A��B)��
(2)д��ͨ��������ĵ缫��Ӧʽ��_________________________________________�����������۲쵽�������ǣ�_________________________________________��
�ο��𰸣���H2(g)+ 1/2O2(g)��H2O(l) ��H��-285.8kJ/mol��2�֣�
��(1)����1�֣�(2) ���淴Ӧ��2�֣���0��x��3��x��3��2�֣��ۣ���2�֣�
�� ��1��B��1�֣� ��2��2Cl--2e-
���������
�����Ѷȣ�����
3��ѡ���� ��ʯī�缫���500mLNaNO3��Cu(NO3)2�Ļ����Һ��ͨ��һ��ʱ��������������ݳ��������ڱ�״���µ�����ֱ�Ϊ11.2L��8.4L����ԭ��Һ��Cu2+�����ʵ���Ũ�ȣ�������Һ��������䣩��
A��1.25 mol?L��1
B��2.5 mol?L��1
C��0.50 mol?L��1
D��1.0 mol?L��1