1、推断题 下图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物。
已知:①反应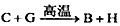 能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:
能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应: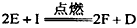 ,F中E元素的质量分数为60%。
,F中E元素的质量分数为60%。
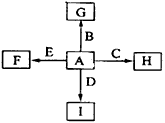
回答问题:
⑴①中反应的化学方程式为____________________;
⑵化合物I的电子式为_______________,它的空间结构是_______________;
⑶1.6gG溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需的铜粉的质量(写出离子方程式和计算过程)_________________;
⑷C与过量NaOH溶液反应的离子方程式为_______________,反应后溶于与过量化合物I反应的离子方程式为_______________________;
⑸E在I中燃烧观察到的现象是_______________。
参考答案:⑴Al+ Fe2O3 Fe+ Al2O3
Fe+ Al2O3
⑵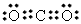 ;直线形
;直线形
⑶2Fe3++Cu=2Fe2++ Cu2+,n(Fe2O3)=0.01mol,依据离子方程式,则n(Cu)= 0.01mol,m(Cu)=0.64g。
⑷2Al + 2OH- + 2H2O==2AlO2- + 3H2↑;AlO2- + CO2 + 2H2O = Al(OH)3↓+ HCO3-
⑸剧烈燃烧,放出热量,生成黑色固体和白色固体
本题解析:
本题难度:一般
2、填空题 (14分)下图中各方框中的字母表示有关的一种反应物或生成物(某些物质略去),其中常温下C为无色液体,B、D、G、I、J为气体,其中B可使湿润的红色石蕊试纸变蓝,A~N的所有物质中只有G为单质,其余为化合物。N为不溶于水的无机酸。

回答下列问题:
(1)A的名称为 ,E的电子式是 ;
(2)写出B + G → I的化学方程式?。
(3)写出Cu与K的稀溶液反应的离子方程式 : 。
: 。
(4)写出G的一种同素异形体的化学式: ,该物质与G在化学性质上的共同点是 。
(5)已知工业上生产0.1molB放出4.62kJ热量,写出该反应的热化学方程式:
。
(6)在反应C+E→G+F中,每生成1.5 molG转移 mol电子。
参考答案:(1)碳酸铵或碳酸氢铵;(2分)?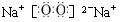 ?(2分)
?(2分)
(2) (2分)
(2分)
(3)3Cu+8H++2NO3-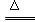 3Cu2++2NO↑+4H2O(2分)
3Cu2++2NO↑+4H2O(2分)
(4)O3(1 分);具有氧化性(1分)
分);具有氧化性(1分)
(5)N2(g)+3H2(g) 2NH3(g);△H=-92.4k J・mol-1(2分)
2NH3(g);△H=-92.4k J・mol-1(2分)
(6)3?(2分)
本题解析:略
本题难度:一般
3、推断题 已知A是灰黑色的硬而脆的固体,B是气态物质,A~E各种物质的相互转化关系如下图所示。
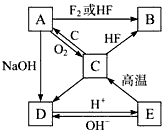
(1)写出B、D、E三种物质的化学式:B_________,D_________,E_________;
(2)画出A的原子结构示意图__________________;
(3)写出C→A的化学方程式__________________。
参考答案:(1)B:SiF4;D:Na2SiO3;E:H2SiO3或H4SiO4
(2)
(3)SiO2+2C Si+2CO↑
Si+2CO↑
本题解析:
本题难度:一般
4、填空题 (13分)已知有以下物质相互转化,其中A为单质
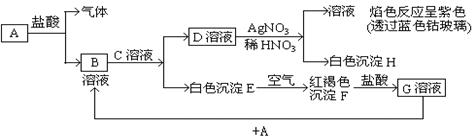
试回答:
(1)写出下列物质的化学式:
A? ?;B?; H?;F?
?;B?; H?;F?
(2)写出由A转变成B的离子反应方程式? ??
??
(3)写出用KSCN溶液鉴别G溶液的离子方程式?
(4)写出G溶液加入A的有关离子反应方程式?
参考答案:(13 分)(1) Fe? FeCl2? AgCl? Fe(OH)3(各1分共4分)
(2)Fe+ 2H+=Fe2+ + H2↑
(3)Fe3++3SCN-=Fe(SCN)3
(4)2Fe3++Fe=3Fe2+?(方程式各3分,)
本题解析:略
本题难度:一般
5、填空题 (共12分)如图转化关系中A―H为中学常见化合物,甲、乙、丙、丁为常见单质,其中甲、丁常温为气体。已知单质乙、化合物A为黄色(或淡黄色)固体。乙经过连续与甲反应后,再与水化合,是工业上制H的反应过程。B、F两种气体都能使澄清石灰水变浑浊。(部分反应物或产物略去)

(1)写出下列反应的化学方程式:
A与B ____________________________________________________
Cu与H ___________________________________________________
F与甲____________________________________________________
(2)写出丙与D溶液反应的离子方程式 _______________________________________
(3)常温时H的浓溶液与丙物质并不能看到明显的反应现象,原因是_________?____
?。
参考答案:(1) 2Na2O2+2CO2 ===2Na2CO3+O2
Cu+2H2SO4(浓)==△="=" CuSO4+SO2↑+2H2O
2SO2+O2 2SO3?(△催化剂)
2SO3?(△催化剂)
(2)2Al+2OH-+2H2O=2AlO2-+3H2↑
(3)铝在浓硫酸表面形成致密的氧化膜,阻止内部金属的反应(或铝在浓硫酸中钝化)
本题解析:此题为物质推断题。。已知单质乙、化合物A为黄色(或淡黄色)固体,故单质乙为硫粉、化合物A为过氧化钠;过氧化钠和水反应生成氢氧化钠和氧气,过氧化钠还能和二氧化碳反应生成碳酸钠和氧气,故甲是氧气、B是二氧化碳、E是碳酸钠、D是氢氧化钠;硫粉和氧气反应首先生成二氧化硫,其也能使澄清石灰水变浑浊,符合题目要求,二氧化硫连续氧化生成三氧化硫,再和水反应生成硫酸,故F是二氧化硫、G是三氧化硫、H是硫酸;硫酸和氢氧化钠都能和单质丙生成常温下为气体的丁,故其金属铝,生成的是丁是氢气;据此可回答(1)A与B反应为:2Na2O2+2CO2 ===2Na2CO3+O2;Cu与H的反应为:Cu+2H2SO4(浓)==△="=" CuSO4+SO2↑+2H2O;F与甲的反应为:2SO2+O2 2SO3?(△催化剂);(2)铝和氢氧化钠溶液反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑;(3)金属铝在浓硫酸表面形成致密的氧化膜,阻止内部金属的反应(或铝在浓硫酸中钝化)
2SO3?(△催化剂);(2)铝和氢氧化钠溶液反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑;(3)金属铝在浓硫酸表面形成致密的氧化膜,阻止内部金属的反应(或铝在浓硫酸中钝化)
本题难度:一般