1��ѡ���� ����˵����ȷ����(NA��ʾ�����ӵ���������ֵ)��?��?
A���ڳ��³�ѹ�£�11.2LN2���еķ�����Ϊ0.5NA
B���ڳ��³�ѹ��,1molHe���е�ԭ����ĿΪNA
C��22.4LCl2����ԭ����Ϊ2NA
D����ͬ��ͬѹ��,��ͬ������κ����嵥������ԭ������ͬ
�ο��𰸣�B
���������A����ȷ�����³�ѹ�£�11.2L���������ʵ�������0.5mol��������1��ԭ�ӹ��ɵģ�����ѡ��Bȷ��C����ȷ����Ϊû��ע�������״̬��D����ȷ����ͬ��ͬѹ��,��ͬ������κ����嵥��������������ͬ����ԭ������һ����ͬ����ѡB��
���������鰢���ӵ�������Ӧ�õ���Ŀ��Ϊ�߿��ؿ���Ŀ�������������ȿ�����ѧ�������ʵ�������������������������밢���ӵ�������ϵ�����⣬�ֿ��Ժ��Ƕ�ǶȵĻ�ѧ֪ʶ���ݡ�Ҫȷ����������Ŀ��һ��Ҫ���պ������ʵ���Ϊ���ĵĸ���ѧ���밢���ӵ������Ĺ�ϵ������ҪȷŪ����ӡ�ԭ�ӡ�ԭ�Ӻ����������Ӽ�������ӵĹ��ɹ�ϵ��
�����Ѷȣ�һ��
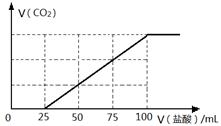
2��ѡ���� ��100 mL NaOH��Һ��ͨ��һ������CO2���壬��ַ�Ӧ������������Һ����μ���0.2 mol/L�����ᣬ����CO2������������������֮���ϵ����ͼ��ʾ�������ж���ȷ����
A��ԭNaOH��Һ��Ũ��Ϊ0.1 mol/L
B��ͨ��CO2�����Ϊ448 mL
C��������Һ�����ʳɷֵ����ʵ���֮��Ϊn(NaOH)��n(Na2CO3) =" 1:" 3
D��������Һ�����ʳɷֵ����ʵ���֮��Ϊn(NaHCO3)��n(Na2CO3) =" 2:" 1
�ο��𰸣�D
�����������0��25mLû���������ɣ���25mL��ʼ���������ɶ�����̼���壬����������100mL��25mL=75mL�������������ĵ���������Ϊ1��3����NaOH��Һͨ��һ����CO2��Ӧ����Һ�е��������ʵ����Ĺ�ϵ��Na2CO3��NaHCO3=1��2��D��ȷ����C������HCl��NaCl��NaOH����NaOH�����ʵ���Ϊ0.1L��0.2mol/L=0.02mol��Na+�����ʵ���Ũ��Ϊ0.02/0.1=0.2mol/L����A������Na2CO3��NaHCO3=1��2����̼ԭ���غ��֪������̼�����ʵ���Ϊ0.075*0.2=0.015mol������������������CO2��������ڱ�״����Ϊ0.015mol��22.4L/mol=336mL��B����
�����Ѷȣ�һ��
3��ѡ���� ���й���ʵ��ԭ��������������������ȷ���ǣ�������
A����ȥ���������е����ᣬ�����ñ��͵�̼������Һ
B��������Һʱ�����ӿ̶��������ݣ���ʹ��������ҺŨ��ƫ��
C��ֽ����ʵ���У���ֽ�ϵ������������ëϸ�����㣬ʹ����������С
D��ʵ���ҿ���������������ͭ����Һ��������ͣ��۲쵽�������dz������ɫ����
�ο��𰸣�D
���������
�����Ѷȣ���
4��ѡ���� ��NAΪ�����ӵ�����������������ȷ����
A��32g��ԭ�ӵ�������������ΪNA
B��1L0.1mol?L-1CaCl2��Һ��Cl-��Ϊ0.1NA
C��1mol�����������������Ϊ16NA
D����״���£�22.4 L�����������Ļ�������еķ�������ΪNA
�ο��𰸣�D
�����������ԭ�ӵ�������������6������32gS�����ʵ�����1mol��������������Ϊ6Na��A����ȷ�������Ȼ��ƵĻ�ѧʽ��֪��1mol�Ȼ����к���2mol�����ӣ�����ѡ��B��Cl-��Ϊ0.2Na��B����ȷ������ķ���ʽ��CH4������10�����ӣ�����1mol�����������������Ϊ10Na��C����ȷ����״���£�22.4 L�����������Ļ����������ʵ�����1mol�����Է�������ΪNa��D��ȷ����ѡD��
�����������ӵ�����������߿��ġ��ȵ㡱���⡣������ȫ���߿���ѧ���������ʼ���Ϊ�������������鰢���ӵ�������Ӧ�õ���Ŀ��Ϊ�߿��ؿ���Ŀ�������������ȿ�����ѧ�������ʵ�������������������������밢���ӵ�������ϵ�����⣬�ֿ��Ժ��Ƕ�ǶȵĻ�ѧ֪ʶ���ݡ�Ҫȷ����������Ŀ��һ��Ҫ���պ������ʵ���Ϊ���ĵĸ���ѧ���밢���ӵ������Ĺ�ϵ������ҪȷŪ����ӡ�ԭ�ӡ�ԭ�Ӻ����������Ӽ�������ӵĹ��ɹ�ϵ�������ķ���˼·�ǣ�����ȷ�����йظ���Ļ����ϣ��������ʵ�������������������Һ��Ũ�ȵ�ת��Ϊָ�����ӵ����ʵ���(mol)�����жϡ�
�����Ѷȣ�һ��
5��ʵ���� ����������Ϊ98%��Ũ����(�ܶ�Ϊ1.84g/cm3)���Ƴ�1mol/L��ϡ����.��ʵ���ҽ���Ҫ��������220mL.�Իش��������⣺
��1������ϡ����ʱ��Ӧѡ������Ϊ________mL������ƿ��
��2����������Ҫ����Ͳ��ȡ________mLŨ���ᣬ����ȡʱ��ѡ��������Ͳ�е�____(����ĸ).
A��5mL�������� B��10mL�������� C��15mL�������� D��50mL
��3������ȡŨ������������в�����
�ٵ�ϡ�͵��������¶�������һ�º��ز�����ע������ƿ�С�
��������ƿ��С�ļ�����ˮ��Һ��ӽ����α���1-2cm�������ý�ͷ�ιܼ�����ˮ��ʹ��Һ�İ�Һ��ײ���ƿ���Ļ��α������С�
����ʢ������ձ���ע������ˮ���������ò�����������ʹ���Ͼ��ȡ�
��������ˮϴ���ձ��Ͳ�����2��3�Σ�����ϴ��Һȫ��ע������ƿ���������У�
��ȷ��˳����(�����)________��
��4��ָ����ʵ���������ĵط�,�����и���____________________
��5�����������ƹ����У��øո�ϴ�ӽྻ����Ͳ����ȡŨ���ᣬ�����Ƶ�ϡ����Ũ�Ȼ�________(�ƫ�ߡ�����ƫ�͡�������Ӱ�족����ͬ).��δ������ˮϴ���ձ��ڱڻ�δ��ϴ��Һע������ƿ�������Ƶ�ϡ����Ũ�Ȼ�________��
�ο��𰸣���1��250
��2��13.6 ��C
��3���ۢ٢ܢ�
��4���۴���Ӧ��Ũ���Ỻ��ע������ˮ��
��5��ƫ�� ��ƫ��
���������
�����Ѷȣ�һ��