1、实验题 (15分)某实验小组同学对电化学原理进行了一系列探究活动。
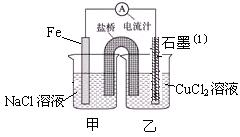
(1)右图为某实验小组依据氧化还原反应:(用离子方程式表示)?设计的原电池装置,一段时间后,两电极质量相差12g,导线中通过?mol电子。
(2)其它条件不变,若将CuCl2溶液换为NH4Cl溶液,石墨电极反应式为?,这是由于NH4Cl溶液显?性,(填酸性、碱性或中性)用离子方程式表示溶液显此性的原因?,用吸管吸出铁片附近溶液少许至于试管中,向其中滴加少量新制饱和氯水,写出发生反应的离子方程式?,然后滴加几滴硫氰化钾溶液,溶液变红,继续滴加过量新制饱和氯水,颜色褪去,同学们对此做了多种假设,某同学的假设是:溶液中的+3价铁被氧化为更高的价态。”如果+3价铁被氧化为FeO42-,试写出该反应的离子方程式?。
(3)如图其它条件不变,若将盐桥换成弯铜导线与石墨相连成n型,如图所示,一段时间后,在甲装置铜丝附近滴加酚酞试液,现象是?,电极反应为?;乙装置中石墨(1)为??极(填正、负、阴、阳),乙装置中与铜线相连石墨电极上发生的反应式为?,产物常用?检验,反应的离子方程式为?。
参考答案:
(1)Fe +Cu2+ ="==" Fe2+ + Cu?(1分)? 0.2mol。(1分)
(2)2H+ + 2e-="==" H2↑;酸(各1分)? NH4+ + H2O  ?NH3・H2O + H+(1分)
?NH3・H2O + H+(1分)
2Fe2+ + Cl2="==" 2Fe3+ + 2Cl-?(1分)?2Fe3++3Cl2+8H2O==2FeO42-?+6Cl-?(2分)
(3)溶液变红(1分)? O2+2H2O+4e―="==" 4OH―(2分)?阴(1分),2Cl――2e―===Cl2↑(1分),
湿润淀粉碘化钾试纸(1分),?Cl2?+ 2I- ="=" 2Cl― ?+I2 (1分)?。
本题解析:略
本题难度:简单
2、实验题 (Ⅰ)某校合作探究小组利用业余时间上网搜索烯类化合物与溴加成反应的有关信息,获得的有关结构与数据列表如下(以乙烯为标准)
烯类化合物
| 相对速率
|
(CH3)2C=CHCH3
| 10.4
|
CH3CH=CH2
| 2.03
|
CH2=CH2
| 1.00
|
CH2=CHBr
| 0.04
|
(1)据表中数据,总结烯类化合物加溴时,反应速率与碳碳双键上取代基的种类、个数间的关系:___________________________?______。
(2)下列化合物与氯化氢加成时,取代基对速率的影响与上述规律类似,其中反应速率最慢的是_________。
A.(CH3)2C=" C" (CH3)2?B.CH3CH=CHCH3? C.CH2=CH2?D.CH2=CHCl
 (Ⅱ)另一合作探究小组根据所学知识归纳整理乙醇、水、苯酚、碳酸( HO―C―OH)、乙酸分子中羟基上氢原子的活泼性。?O?
(Ⅱ)另一合作探究小组根据所学知识归纳整理乙醇、水、苯酚、碳酸( HO―C―OH)、乙酸分子中羟基上氢原子的活泼性。?O?
(1)甲同学将一些化学实验收集整理如下:
A.金属钠分别与水和乙醇反应? B.苯酚、二氧化碳、乙酸分别与氢氧化钠溶液反应
C.向二氧化碳水溶液、乙酸溶液中分别滴加紫色石蕊试液
D.将鸡蛋壳破碎后加入到醋酸溶液中? E.向苯酚溶液中滴加FeCl3溶液
F.向苯酚钠溶液中分别通入二氧化碳和滴加盐酸
其中能说明水比乙醇强的是?(填字母,下同),乙酸比碳酸强的是?。
(2)乙同学与其他同学合作,设计了一个简单的一次性完成的实验装置来验证乙酸、碳酸和苯酚溶液的酸性强弱,以说明其羟基上氢原子的活泼性顺序。根据下列实验装置图回答有关问题。
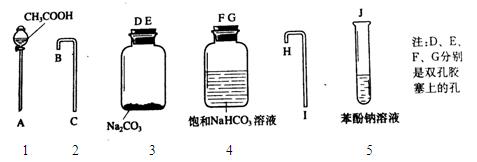
① A对应的仪器名称是?;
② 各仪器的连接顺序是(填数字,仪器可重复使用)?;
③ 饱和NaHCO3溶液作用是?;
④ 实验过程中观察到的现象有?。
参考答案:(12分)(Ⅰ)(1)甲基使反应速率加快,溴原子使反应速率减慢、甲基数目越多反应速率越快(2分)?(2)D (1分)
(Ⅱ)(1)A,D(各1分,共2分)(2)①分液漏斗(1分)②1-2-3-2-4-2-5(2分)
③除掉CO2中的乙酸气体(2分)④碳酸钠固体表面有气泡放出;苯酚钠溶液变浑浊;
插入饱和NaHCO3溶液的导管口有气泡放出(2分,只要答出前两个现象就得满分
本题解析:略
本题难度:一般
3、选择题 化学变化在我们生活中处处可见,利用家庭生活用品不能够完成的探究性实验是(?)
A.检验自来水中含有Cl-
B.检验鸡蛋壳中含有碳酸盐
C.检验加碘食盐中加的不是碘单质
D.除去热水瓶中的水垢
参考答案:A
本题解析:检验Cl-需要药品硝酸银,生活中难于得到。B碳酸盐可用食醋检验,C碘单质可用淀粉溶液来检验,D水垢可以用食醋来除。
本题难度:一般
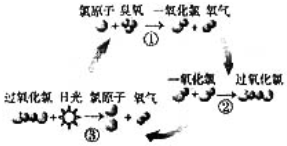
4、选择题 1995年三位美国科学家因在氟利昂和臭氧层方面的工作获得诺贝尔化学奖,他们的研究揭示了大气中臭氧层被破坏的机理,由图可知( )
A.日光在反应中做催化剂
B.过氧化氯是一种很稳定的物质
C.过氧化氯的结构式为O-Cl-Cl-O
D.臭氧分子最终转变为氧气分子