1、实验题 某同学为了探究该校化学实验室的一种黑色粉末和一瓶标签破损的无色溶液,可能是什么物质,大胆猜想并设计实验进行验证。
[发现问题]当把黑色粉末与无色溶液混合时即产生气泡。[查阅资料]中学化学实验室常见的黑色粉末有氧化铜、二氧化锰、四氧化三铁、铁粉、炭粉等。
[提出假设]黑色粉末是?,无色溶液是?。(只写一种假设)
[设计实验]
?
参考答案:二氧化锰,过氧化氢(合理都可以)
本题解析:
实验操作
实验现象
实验结论
向盛有少量黑色粉末的试管中加入适量的无色溶液;用排水法收集一试管气体。
然后用带火星的木条伸入收集气体的试管中。
带火星的木条复燃
此气体是氧气,原假设成立(
本题难度:一般
2、实验题 (18分)某研究性学习小组在CO还原Fe2O3的实验中,用磁铁吸出生成的黑色粉末X,他们认为X不一定是Fe,若温度不均时会生成Fe3O4,也能被磁铁吸引。为了探究X的组成,他们进行了如下实验。
I、定性检验
实验编号
| 实验操作
| 实验现象
|
①
| 取少量黑色粉末X放入试管1中,注入浓盐酸,微热
| 黑色粉末逐渐溶解,溶液呈黄绿色,有少量气泡产生
|
②
| 另取少量黑色粉末X放入试管2中,注入足量硫酸铜溶液,振荡,静置
| 有极少量红色物质析出,仍有较多黑色固体未溶解
|
由上述实验现象推断,黑色粉末X的成分是?。
II定量测定

⑴操作Z的名称是?。
下列仪器中,在灼烧沉淀时必须用到的是?(填字母)。
 ?
?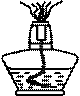

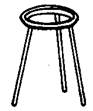
A? B? C? D? E? F
⑵写出溶液Y中滴加H2O2溶液时发生反应的离子方程式?。
⑶将沉淀物加热,并置于干燥器中冷却至室温,用托盘天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2g,若b1―b2 = 0.3g,则接下来还应进行的操作是
? ?。
?。
⑷有同学认为:上述流程若不加入H2O2,其它步骤不变,只要在空气中充分放置仍可达到目的。他的理由是?。(用化学方程式表示)
⑸通过以上数据,得出2.376g黑色粉末中各成分的物质的量为?。
参考答案:除(5)是4分, 方程式各3分,其他每空2分
Ⅰ? Fe 、 Fe3O4(2分)
Ⅱ(1)过滤、洗涤 (只选过滤得1分)?A C E F(2分)
(2)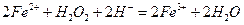 (3分)
(3分)
(3)再次加热 并置于干燥器中冷却,称量,直至两次的质量差不超过0.1g为止。(2分)
并置于干燥器中冷却,称量,直至两次的质量差不超过0.1g为止。(2分)
(4)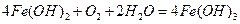 (3分)
(3分)
(5)n(Fe)=0.001mol(2分)? n(Fe3O4)=0.01mol(2分)
本题解析:略
本题难度:一般
3、选择题 有机物的天然提取和人工合成往往得到的是混合物,假设给你一种这样的有机混合物让你研究,一般要采取的几个步骤是
[? ]
A.分离、提纯→确定化学式→确定实验式→确定结构式
B.分离、提纯→确定实验式→确定化学式→确定结构式
C.分离、提纯→确定结构式→确定实验式→确定化学式
D.确定化学式→确定实验式→确定结构式→分离、提纯
参考答案:B
本题解析:
本题难度:一般
4、实验题 化学兴趣小组对用铜制取硫酸铜晶体的实验方案作研究。甲组同学将铜粉投入盛有稀硫酸的容器中,不发生反应。他们向容器底部缓缓鼓入氧气,溶液慢慢变蓝色,若在溶液中置一些铂丝,反应速率明显加快。此时,其他组的同学提出方案如下:
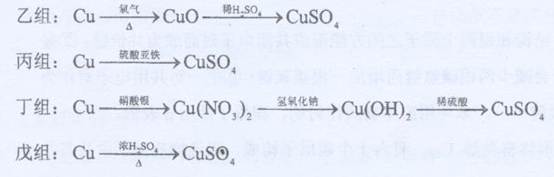
(1)甲组实验可用一个化学反应方程式表示为?,使反应变快的可能原因是?。
(2)在五个方案中,科学性有错的是?组方案,经济性最差的是?组方案。
(3)可持续发展的原则要求化工生产①能耗尽量低,这应排除使用?组方案;②无污染,这应排除?组方案。
(4)相对能耗低,污染小的是?组方案。该给从反应器中排出的溶液中(含有少量H2SO?4?以抑制水解)取得产品的实验操作步骤应为?、?、?,对取得产品后残留物质的处理方法是?。
参考答案:
(1)2Cu+O2+2H2SO4→2CuSO4+2H2O,形成了原电池
(2)丙,丁,
(3)乙戊,戊
(4)甲,加热蒸发、冷却结晶、过滤并洗涤晶体,循环使用。
本题解析:
本题考查实验探究。(1)通入的氧气作为氧化剂,在溶液中置一些铂丝,与铜形成原电池,反应速率加快;(2)铜与Fe2+不反应,丙方案错误;丁方案所需要的原料很多,反应步骤太多,且费用很大,经济效益很差;(3)要求能耗尽量低,则必须在常温下进行,乙戊排除;要求无污染,排除戊,戊方案可以产生SO2;(4)甲方案不需加热,且没有污染性气体产生为最佳方案。
本题难度:一般
5、实验题 (12分)某学生在实验室测定一未知浓度的稀盐酸,已知在25ml氢氧化钠标准溶液中逐滴加入0.2mol/L醋酸溶液的PH变化曲线如图所示:
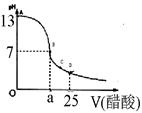
(1)该氢氧化钠溶液的物质的量浓度为??mol.L―1
(2)在B点,a?12.5ml(填“>”、“<”或“="”" )。
(3)配制100 mL NaOH标准溶液所需仪器除托盘天平、玻璃棒、胶头滴管外,还需要?
(4)用 ?量取20.00 mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用NaOH标准溶液进行滴定。为了减小实验误差,该同学一共进行了三次实验,假设每次所取稀盐酸体积均为20.00 mL,三次实验结果记录如下:
实验次数
| 第一次
| 第二次
| 第三次
|
消耗NaOH溶液体积/mL
| 19.00
| 23.00
| 23.02
|
该盐酸的浓度约为___________________ (保留两位有效数字)。
滴定达到终点的标志是??
参考答案:(共12分)
(1)0.1mol/L?(2)>?(3)烧杯、100mL容量瓶(答对一个得1分)
(4)酸式滴定管? 0.12 mol・L―1?最后一滴氢氧化钠溶液加入,溶液由无色恰好变成浅红色,半分钟内不褪色
本题解析:略
本题难度:简单