|
高中化学知识点归纳《化学反应与能量》高频考点巩固(2020年模拟版)(十)
2020-08-23 07:48:03
【 大 中 小】
|
1、选择题 25℃、101 kPa下,2g氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是( )
A.2H2(g) + O2(g) ="=" 2H2O(1) △H=
|
参考答案:
本题解析:
本题难度:一般
2、选择题 下列物质中,既有离子键又有共价键的是(?)
A.Ca(NO3)2
B. KOH
C. H2O
D. NH4F
参考答案:ABD
本题解析:一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间容易形成共价键,据此可知,A、B、D中含有离子键和共价键。C中含有共价键,因此答案选ABD。
点评:该题是高考中的常见考点,属于中等难度试题的考查,试题基础性强,侧重对学生基础知识的训练,主要是考查学生灵活运用化学键知识解决实际问题的能力。该题的关键是明确离子键、共价键的含义和判断依据,然后结合题意灵活运用即可。有利于提高学生的应试能力。
本题难度:简单
3、实验题 已知25℃、101 kPa下,稀的强酸与强碱溶液反应的中和热为57.3 kJ/mol。
(1)写出表示稀硫酸与稀烧碱溶液发生反应的中和热的热化学方程式: 。
(2)学生甲用稀硫酸与稀烧碱溶液测定中和热装置如图。
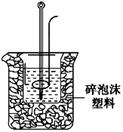
①实验时所需的玻璃仪器除烧杯、量筒外还需: 。
②该装置中有一处错误是: ,如果用该错误装置测定,结果会 (填“偏高”“偏低”“无影响”)
③如果,该生用50 mL 0.25 mol/L的稀硫酸与50 mL 0.55 mol/L的稀烧碱溶液,他用试剂的用量的理由是: 。在该实验中需要测定某种数据,完成一次实验,需要测定该数据的次数为 次。
④若反应前溶液以及中和后的混合液的密度均设为 1 g/cm3,混合前酸与碱的温度均为t1,混合后溶液的温度为t2,比热容为 4.18 J/(g・℃)。那么该生测定中和热:ΔH= 。
(3)学生乙用2 mol/L的硫酸来测定与锌粒和锌粉反应的快慢,设计如图(Ⅰ)装置:
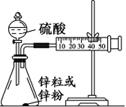 
图Ⅰ 图Ⅱ
①该生两次实验测定时间均设定为10 min,那么他还要测定的另一个数据是:
。
②如果将图Ⅰ装置中的气体收集装置改为图Ⅱ,实验完毕待冷却后,该生准备读取滴定管上液面所处的刻度数,发现滴定管中液面高于干燥管中液面,应先采取的操作是: 。
③该实验结果中,你估计与酸反应较快的是 。
参考答案:(1)1/2H2SO4(aq)+NaOH(aq)=1/2Na2SO4(aq)+H2O ΔH=-57.3 kJ/mol
(2)① 温度计、环形玻璃搅拌棒
② 未用硬纸板(或塑料板)盖住烧杯 偏低
③ 保证硫酸完全反应 3
④ kJ/mol kJ/mol
(3)①测定相同条件下氢气的体积
②向下移动滴定管,直到两边液面相平
③锌粉
本题解析:(1)中和热是在一定条件下,稀溶液中,强酸和强碱反应生成1mol水时所放出的热量,所以该反应的热化学方程式是1/2H2SO4(aq)+NaOH(aq)=1/2Na2SO4(aq)+H2O ΔH=-57.3 kJ/mol。
(2)①由于需要测量溶液的温度以及反应还需要搅拌,所以还缺少的玻璃仪器有温度计、环形玻璃搅拌棒。
②根据装置图可知实验中没有用硬纸板(或塑料板)盖住烧杯,这样就会导致热量的损失,实验测定结果会偏低。
③氢氧化钠过量可以保证硫酸完全反应,从而减少实验误差。实验中需要测量的数据是溶液的温度,因此至少需要测量3次,即反应前酸和碱的溶液温度,以及反应后溶液的温度。
④溶液的质量是100g,反应中放出的热量是100×4.18×(t2-t1)J=0.418(t2-t1)kJ。由于反应中有0.025mol的水生成,所以中和热= kJ/mol。 kJ/mol。
(3)①要比较反应速率的大小,除了测量时间外,还需要测定相同条件下生成氢气的体积。
②由于气体的体积受温度和压强的影响,所以必须保证气体的压强和大气压是相同的,因此正确的操作是向下移动滴定管,直到两边液面相平。
③由于锌粉的表面积大,反应速率快,即反应速率较快的是锌粉。
考点:考查热化学方程式的书写、中和热的测定以及影响反应速率的因素等
点评:化学是一门以实验为基础的学科,所以有化学实验即科学探究之说法。化学实验综合性强,理论和实践的联系紧密,有的还提供一些新的信息,要求学生必须扎实的基础,并且通过进行知识的类比、迁移、重组,全面细致的思考才能正确解答。
本题难度:困难
4、选择题 使0.15molMnO2与过量的12mol・L-1的浓盐酸反应,使50mL12mol・L-1的浓盐酸与足量MnO2反应,两者产生的氯气相比(其他条件相同)。
A.一样多
B.前者较后者多
C.后者较前者多
D.无法比较
参考答案:B
本题解析:试题分析:由于二氧化锰在和浓盐酸的反应过程中,盐酸的浓度会逐渐降低。而稀盐酸不能被氧化生成氯气,所以前者较后者生成的氯气多,答案选B。
考点:考查氯气的制备及有关计算
点评:本题属于高考中的常见题型,试题难度不大。主要是有利于培养学生严谨、客观的思维方法,有利于调动学生的学习积极性,提高学习效率。
本题难度:困难
5、选择题 下列说法正确的是
A.放热反应发生时不必加热,吸热反应在加热后才能发生
B.反应热指的是反应过程中放出的热量
C.反应热的大小与反应的途径有关,无论是一步完成还是分几步完成,其反应热基本相同
D.依据盖斯定律,热化学方程式具有加合性,也可以进行加、减、乘、除四则运算
|