1、填空题 工业上以黄铜矿(主要成分是CuFeS2,杂质不溶于水和酸)为原料,制备蓝色晶体G,其化学式为[Cu(NH3)4]SO4・H2O,涉及流程如下:

已知25℃时,几种金属氢氧化物的溶度积常数和完全沉淀的pH范围如下表:
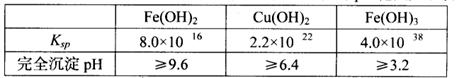
(1)黄铜矿在空气中焙烧能生成铁和铜的低价硫化物,写出其反应的化学方程式:?;
(2)试剂X的化学式为?;
(3)常温下,0.1 mol/L试剂Y的pH=11,则该温度下,试剂Y的电离常数为?,用pH试纸测该溶液pH值的方法是?;
(4)在溶液N中加入乙醇的目的是?。
2、填空题 (10分)回答下列关于铁元素及其化合物的知识:
(1)除去铁粉中混有的铝粉可以选用的试剂为?(填序号)。
A.稀盐酸? B.氢氧化钠溶液? C.浓硫酸
(2)在常温下,铁与水并不起反应,但在高温下,铁与水蒸气可发生反应。
该反应的化学方程式?;
该反应中的还原剂是?,氧化剂是?。
(3)实验室在保存FeCl2溶液时为了防止FeCl2溶液变质,经常向其中加入铁粉,其原因是(用离子方程式表示)?。
3、实验题 (16分)铜与浓硫酸反应,实验装置如图所示。
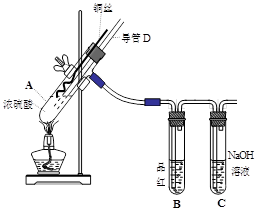
(1) 装置A中发生反应的化学方程式为:?,反应过程中试管B中的现象是?,试管C的作用是?。
(2) 导管D的下端(虚线段)应位于?(液面上、液面下),导管D的作用有:①实验结束后排除装置中的SO2;②?。
实验中发现试管内除了产生白色固体外,在铜丝表面还有黑色固体甲生成,甲中可能含有CuO、Cu2O、CuS、Cu2S。为探究甲的成分,进行了以下的实验。
查阅资料可知:Cu2O + 2HCl =CuCl2+ Cu + H2O, 2Cu2O + O2煅烧 4CuO,2CuS+3O2煅烧2CuO+2SO2,Cu2S+2O2煅烧2CuO+SO2。CuS、 Cu2S和稀HCl不反应。
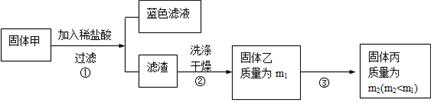 (3) 固体乙在空气中煅烧时,使用的实验仪器除了玻璃棒、三脚架、酒精灯外,还必须有:?。
(3) 固体乙在空气中煅烧时,使用的实验仪器除了玻璃棒、三脚架、酒精灯外,还必须有:?。
(4) 煅烧过程中,除上述反应外,还可能发生反应的方程式为?。
(5)结论:甲中有CuO,还肯定含有的物质是?。
4、填空题 生锈的铁钉与过量的盐酸发生反应的离子方程式为____________。
5、选择题 向硫酸亚铁与硫酸铝的混合溶液中加入足量的浓氨水,在空气中滤出所得沉淀,经洗净、干燥、灼烧,最终得到固体的成分是( )
A.Fe2O3、A12O3
B.Fe(OH)2、Al(OH)3
C.Fe(OH)3、A1(OH)3
D.FeO、A12O3