1、填空题 黄铁矿主要成分是FeS2。某硫酸厂在进行黄铁矿成分测定时,取0.1000 g样品在空气中充分燃烧,将生成的SO2气体与足量Fe2(SO4)3溶液完全反应后,用浓度为0.02000 mol・L-1的K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液25.00 mL。
已知:
SO2+2Fe3++2H2O = SO42-+2Fe2++4H+
Cr2O72-+6Fe2++14H+ = 2Cr3++6Fe3++7H2O
(1)样品中FeS2的质量分数是(假设杂质不参加反应)________________。
(2)若燃烧6g FeS2产生的SO2全部转化为SO3气体时放出9.83 kJ热量,产生的SO3与水全部化合生成
H2SO4,放出13.03 kJ热量,写出SO3气体转化为H2SO4的热化学方程式__________________________。
(3)煅烧10 t上述黄铁矿,理论上产生SO2的体积(标准状况)为_________L,制得98%的硫酸质量为____t,SO2全部转化为H2SO4时放出的热量是___________kJ。
参考答案:(1)90.00%
(2)SO3(g)+H2O(l)==H2SO4(l);△H=-130.3 kJ/mol
(3)3.36×106;15;3.43×107
本题解析:
本题难度:一般
2、填空题 (10分).工业合成氨与制备硝酸一般可连续生产,流程如图所示:

(1)工业生产时,制取氢气的一个反应为:CO+H2O(g) CO2+H2
CO2+H2
T℃时,往1L密闭容器中充入0.2mol CO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol・L-1。该温度下此反应的平衡常数K=_____(填计算结果)。
(2)合成塔中发生反应N2(g)+3H2(g) 2NH3(g);△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1____573K(填“>”、“<”或“=”)。
2NH3(g);△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1____573K(填“>”、“<”或“=”)。
T/℃
| T1
| 300
| T2
|
K
| 1.00×107
| 2.45×105
| 1.88×103
|
(3)N2和H2以铁作催化剂从145℃就开始反应,不同温度下NH3的产率如图所示。
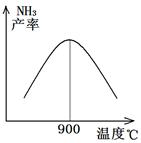
温度高于900℃时,NH3产率下降的原因是 。
(4)硝酸厂的尾气直接排放将污染空气,目前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g); △H=-574kJ・mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g); △H=-1160kJ・mol-1
则甲烷直接将NO2还原为N2的热化学方程式为:
(5)氨气在纯氧中燃烧,生成一种单质和水。科学家利用此原理,设计成氨气-氧气燃料电池,则通入氨气的电极碱性条件下发生反应的电极反应式为 。
参考答案:(1)1(2分); (2)< (2分)(3)温度高于>900℃时,平衡向左移动(2分)
(4) CH4(g)+2NO2(g)=CO2(g)+2H2O(g)+N2(g) ΔH=-867KJ/mol; (2分)
(5) 2NH3-6e-+6OH-=N2+ 6H2O (2分)
本题解析: (1)CO + H2O(g) CO2 + H2
CO2 + H2
C开始(mol/L) 0.2 0.3 0 0
C改变(mol/L)0.12 0.12 0.12 0.12
C平衡(mol/L)0.08 0.18 0.12 0.12
所以平衡常数K=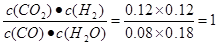 ;
;
(2)由于反应N2(g)+3H2(g) 2NH3(g)的正反应是放热反应,升高温度,根据平衡移动原理,化学平衡向吸热反应方向移动,即对该反应来说,平衡向逆反应方向移动,所以化学平衡常数减小,由于在温度是T1时的平衡常数1.00×107大于300℃时的平衡常数2.45×105,所以T1<300℃;
2NH3(g)的正反应是放热反应,升高温度,根据平衡移动原理,化学平衡向吸热反应方向移动,即对该反应来说,平衡向逆反应方向移动,所以化学平衡常数减小,由于在温度是T1时的平衡常数1.00×107大于300℃时的平衡常数2.45×105,所以T1<300℃;
(3)N2和H2以铁作催化剂从145℃就开始反应,在不同温度下NH3的产率如图所示,在温度高于900℃时,NH3产率下降的原因是温度高于>900℃时,升高温度,平衡向左移动,所以NH3的平衡含量减小,因此产率降低;
(4)(①+②)÷2,整理可得:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g); ΔH=-867KJ/mol;
(5)在氨气-氧气燃料电池中,通入氨气的电极是负极,则碱性条件下发生反应的电极反应式为2NH3-6e-+6OH-=N2+ 6H2O。
考点:考查化学平衡常数的计算、温度对化学平衡移动的影响、热化学方程式及原电池电极式的书写。
本题难度:困难
3、选择题 已知 ,1molH2S发生该反应所放出的热量为硫化氢的燃烧热,则X为
,1molH2S发生该反应所放出的热量为硫化氢的燃烧热,则X为
[? ]
A.S(s)
B.SO2(g)
C.SO3(g)
D.SO3(s)
参考答案:B
本题解析:
本题难度:简单
4、选择题 1gH2完全燃烧生成液态水放出142.9KJ热量,下列反应的热化学方程式正确的是
[? ]
A.H2 + O2=2H2O △H= -571.6KJ/mol
B.H2(g)+1/2O2(g)= H2O (l) △H= -142.9KJ/mol
C.H2(g)+1/2O2(g)= H2O (l) △H= -285.8KJ/mol
D.2H2(g) + O2(g) = 2H2O (g) △H= -571.6KJ/mol
参考答案:C
本题解析:
本题难度:简单
5、选择题 热化学方程式C(s)+H2O(g)
?CO(g)+H2(g);△H=+131.3kJ/mol表示( )
A.碳和水反应吸收131.3kJ能量
B.1mol碳和1mol水反应生成一氧化碳和氢气并吸收131.3kJ热量
C.1mol固态碳和1mol水蒸气反应生成一氧化碳气体和氢气,并吸热131.3kJ
D.1个固态碳原子和1分子水蒸气反应吸热131.1kJ
参考答案:C
本题解析:
本题难度:简单