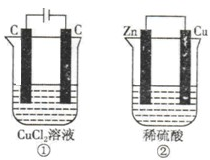
1��ѡ���� ��һ����ȼ�ϵ�أ����������������缫����KOH��Һ�У�Ȼ����X��ͨ��CH4����Y��ͨ��O2�����ڴ�ȼ�ϵ�ص�˵��������ǣ�?��
A��ͨ��CH4��X���Ǹ�����ͨ��O2��Y��������
B���ŵ�һ��ʱ��������Һ��KOH�����ʵ�������
C���ڱ�״���£�ͨ��5.6 LO2����ȫ��Ӧʱ��1.0 mol����ת��
D���ŵ�ʱ��ͨ�����һ��������pH����
�ο��𰸣�BD
������������������֪�����飭����ȼ�ϵ�ص��ܷ�ӦΪ��CH4��2O2��2KOH=K2CO3��3H2O����ͨ�����һ��������KOH�����pH�ؽ��ͣ�KOH�����ʵ����ؼ�С����������ӦʽO2��2H2O��4e��=4OH����֪��������O2�� ��0.25molʱ��ת�Ƶ�
��0.25molʱ��ת�Ƶ�
�ӵ����ʵ���Ϊ4��0.25mol��1.0mol��
�����Ѷȣ�һ��
2��ѡ���� ����������ȷ����
A���ϳɰ����������н�NH3Һ�����룬�ɼӿ�����Ӧ���ʣ����N2��H2��ת����
B����1 mol Ba(OH)2��ϡ��Һ�ͺ�1 mol H2SO4��ϡ��Һ��Ӧ�ͷ�����akJ�����ʾ�÷�Ӧ�к��ȵ��Ȼ�ѧ��Ӧ����ʽΪ��
OH��(aq)��H��(aq)=H2O(l) ?H =" -a" kJ��mol��1
C����⾫��ͭʱ��ͬһʱ���������ܽ�ͭ����������������ͭ������С
D������2HI(g)  H2(g)+I2(g)ƽ����ϵ������ƽ����ϵ��ѹǿ��ʹ��ɫ���������������ԭ�����͡�
H2(g)+I2(g)ƽ����ϵ������ƽ����ϵ��ѹǿ��ʹ��ɫ���������������ԭ�����͡�
�ο��𰸣�C
���������A���ϳɰ����������н�NH3Һ�����룬���ܼӿ�����Ӧ���ʣ�����B��Ba(OH)2��H2SO4��Ӧ����BaSO4������H2O���÷�Ӧ�ķ�Ӧ�Ȳ����к��ȣ�����C����⾫��ͭ����������Cuʧ���ӣ����б�ͭ���õ�п��������ʧ���ӣ���ȷ��D���÷�Ӧ�����ϵ�����䣬����ƽ����ϵ��ѹǿ��ƽ�ⲻ�ƶ�������������ԭ���أ�����
�����Ѷȣ�һ��
3������� (11��)��֪��������Խ���γ�ԭ���ʱԽ���ŵ硣�������ͼװ�ã��ش��������⣺
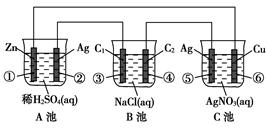
��1����װ�������ǣ�A��________��B��______��C��________��
��2��д���缫�Ϸ����ķ�Ӧ����_____________����___________����_____________��
��3������·����2 mol��������ʱ���ټ��������仯______g�����������仯______g��
��4����Ӧ����һ��ʱ���A��B��C�����е������ҺŨ�Ȳ������________��
�ο��𰸣���1��ԭ��ء����ء���Ƴ�?��2��Zn��2e��==Zn2����2Cl����2e��==Cl2����Ag��e��==Ag����
��3��65��216����4��C��
������������������缫��ԵIJ���������Zn��Ag,����A����ԭ��ء�Zn�Ǹ���������������Ӧ��AgΪ�������������Ϸ�����ԭ��Ӧ�������������˵�ǵ�Դ��B���ǵ��أ�C���ǵ��ء�����Ag�缫���Դ���������ӣ���������Cu�����Դ�ĸ������ӵģ�����������˸ó�Ҳ���ǵ�Ƴء���2������Zn�缫�Ϸ�����Ӧ: Zn��2e��==Zn2��;�ڢ۵缫��Cl���ŵ磬�缫��Ӧʽ��2Cl��-2e-= Cl2�����ڢ�������Ag�������������ǵ���Agʧȥ���ӣ��缫��Ӧʽ��Ag��e��==Ag������3������·����2 mol��������ʱ����ΪZn��+2�۵Ľ�����������1mol��Zn����������Ӧ�����Ԣټ������������65g���ڢ��ϻ��������仯2mol��Ag���õ����ӣ�����ԭ����������Ag,������Ϊ2mol��108g/mol=216g����4����Ӧ����һ��ʱ���A�صĵ������Һ������H2SO4��ΪZn SO4;B�ػ���ΪNaOH��Һ������C����Ϊ��������Ag�����ӣ�����������Ag���õ����ӣ�����ԭ��������Ȼ��AgNO3��Һ�� Ũ�Ȼ������䡣ѡ��ΪC��
�����Ѷȣ�һ��
4��ѡ���� ��ͥ���������õ��������������������������������
A.��ˮϴ�Ӻ���
B.��ˮϴ�Ӻ�δ����
C.������δϴ��
D.����ˮ��
�ο��𰸣�B
���������
�����Ѷȣ�һ��
5��ѡ���� ��ͼ��ʾ������ʵ��װ�ã���Һ�������Ϊ200mL����ʼʱ�������Һ��Ũ�Ⱦ�Ϊ0.1mol/L������һ��ʱ���õ����о�ͨ��0.02mol���ӣ����������ε�ˮ�����Һ������仯��������������ȷ���ǣ�������
A�����������������٣���
B����Һ��pH�仯���ټ�С��������
C���缫���������ʵ���������=��
D���缫��Ӧʽ����������2Cl--2e-�TCl2�������и���2H++2e-�TH2��