1������� ��ͼ�У� ��ʾ��ԭ�ӣ�
��ʾ��ԭ�ӣ�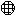 ��ʾ��ԭ�ӡ����ݴ�ͼ����Ӻ�ۡ�����������д����õĻ�ѧ��Ϣ�����ɲ�������Ҳ�ɲ��䣩
��ʾ��ԭ�ӡ����ݴ�ͼ����Ӻ�ۡ�����������д����õĻ�ѧ��Ϣ�����ɲ�������Ҳ�ɲ��䣩
��1��_____________________________________________
��2��_____________________________________________
��3��_____________________________________________
��4��_____________________________________________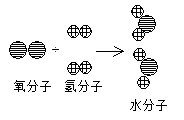
2������� ��12�֣�������Ԫ��A��B��C��D��AԪ�ص�ԭ�����������Ų�Ϊns1��BԪ�ص�ԭ�Ӽ۵����Ų�Ϊns2np2��CԪ�ص�����������������Ӳ�����3����DԪ��ԭ�ӵ�M���Ӳ��P�������3��δ�ɶԵ��ӡ�
��1��Cԭ�ӵĵ����Ų�ʽΪ?����AΪ�ǽ���Ԫ�أ���ԭ�ӹ�����ص���ʽ��A��C�γɵĻ������еĹ��ۼ�����?������ҡ��С�����
��2����n=2ʱ��Bλ��Ԫ�����ڱ��ĵ�?����?�壬BC2����?���ӣ�����ԡ��Ǽ��ԡ�������n=3ʱ��B��C�γɵľ�������?���塣
3������� ±�ػ�ѧ�ḻ��ʣ����γ�±���±�ػ������±����ȶ������͵Ļ����
��1����̬��ԭ�ӵļ۵����Ų�ʽΪ?��
��2��±�ػ�������IBr��ICl����±�ص��ʽṹ���ơ������������Cl2��IBr��ICl�ķе��ɸߵ��͵�˳��Ϊ?��
��3����̬�������д��ڶ��۷���(HF)2����������?��
��4����Ϊ�ȵ���������֮��ṹ���ơ�I3+���ڶ�±�������ӣ�����VSEPRģ���Ʋ�I3+�Ŀռ乹��Ϊ?������ԭ���ӻ�����Ϊ?��
��5����HClO4����HIO4����H5IO6�ۿ�д��(HO)5IO�ݵ�������ǿ������˳��Ϊ?������ţ���
��6��±����RbICl2�ڼ���ʱ��ֽ�Ϊ��������Խϴ��±����A��±�ػ������±�ص��ʣ�A�Ļ�ѧʽ?��
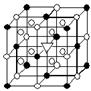
��7����ͼ��ʾΪ±�������ʯ����ѧʽΪNa3AlF6���ľ�����ͼ�С�λ�ڴ������嶥������ģ���λ�ڴ��������12������е��8��С����������ģ�����ͼ�С��е�һ�֡�ͼ�С�ֱ�ָ����������?��?��������������Ĵ�������������?��
4��ѡ���� ���������������ӻ��������(? )
A��NaOH
B��CO
C��Br2
D��H2SO4
5��ѡ���� �����������ڹ��ۻ��������
[? ]
A.C60
B.CaCl2
C.KF
D.C6H6