|
|
|
高考化学知识点归纳《气体的净化、干燥、吸收与收集》考点特训(2020年冲刺版)(七)
2020-08-23 08:25:02
【 大 中 小】
|
1、实验题 S2Cl2是工业上常用的硫化剂,实验室制备的方法有2种:
 已知在S2Cl2中硫元素显+1价,电子式: 已知在S2Cl2中硫元素显+1价,电子式: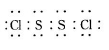 ,它不稳定,在水中易发生歧化反应 (一部分硫元素价态升高,一部分降低)。反应涉及的几种物质的熔沸点如下: ,它不稳定,在水中易发生歧化反应 (一部分硫元素价态升高,一部分降低)。反应涉及的几种物质的熔沸点如下:

实验室利用下列装置制备 (部分夹持仪器已略去):
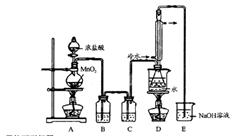
回答下列问题:
(1)写出A装置中发生反应的离子方程式??
(2)实验中盐酸通常采用36.5%的浓溶液,不用稀盐酸的理由是?
(3)D中冷凝管起到导气和冷凝回流双重作用。这种冷却装置可应用于下列高中化学中?实验。
A.石油分馏
B.制备乙烯
C.制取乙酸乙酯
D.制取溴苯
| (4)B装置中盛放的是?,反应结束后从锥形瓶内混合物中分离出产品的方法是?,D中采用热水浴加热的原因是?
(5)A装置仪器装配时,整套装置装配完毕后,应先进行?,再添加试剂。实验完毕,拆除装置时,应先将E中长导管移开液面,目的是??
(6)实验过程中,若缺少C装置,则发现产品浑蚀不清,出现该现象的原因可用化学方程式表示为?。实验完毕,当把剩余浓盐酸倒人E烧杯中与吸收了尾气的氢氧化钠溶液混合时,发现有少量黄绿色刺激性气体产生,产生该现象的原因是?(用离子方程式表示)。
2、选择题 某化学小组用如图所示装置制取氯气。下列说法不正确的是
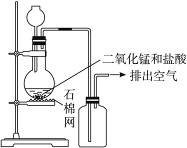
A.该装置图中至少存在三处明显错误
B.该实验中收集氯气的方法不正确
C.为了防止氯气污染空气,必须进行尾气处理
D.在集气瓶的导管口处放一片湿润的淀粉碘化钾试纸可以证明是否有氯气逸出
3、实验题 (9分)孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuSO4・5H2O及CaCO3,步骤如下:
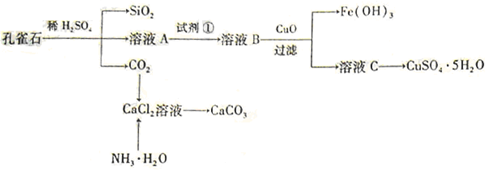
请回答下列问题:(1)溶液A的金属离子有Cu2+、Fe2+、Fe3+。从下列所给试剂中选择:实验步骤中试剂①为 (填代号 ),检验溶液A中Fe3+的最佳试剂为 (填代号)。 ),检验溶液A中Fe3+的最佳试剂为 (填代号)。
a.KMnO4 b.(NH4) 2S? c.H2O2? d.KSCN
(2)由溶液C获得CuSO4・5H2O,需要经过加热蒸发、 、过滤等操作。除烧杯、漏斗外,过滤操作还用到另一玻璃仪器,该仪器在此操作中的主要作用是 。
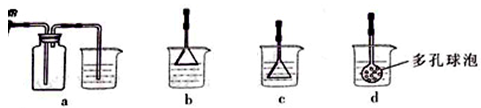
(3)由框图可知制备CaCO3时,应向CaCl2溶液中先通入(或先加入) (填化学式)。若实验过程中有氨气逸出,应选用下列 装置回收(填代号)。
(4 )欲测定溶液A中Fe2+的浓度,需要用容量瓶配制某标准溶液,定容时俯视容量瓶的刻度线,会使配制的浓度?。(填“偏高”、“偏低”、“无影响”。) )欲测定溶液A中Fe2+的浓度,需要用容量瓶配制某标准溶液,定容时俯视容量瓶的刻度线,会使配制的浓度?。(填“偏高”、“偏低”、“无影响”。)
4、实验题 (16分)乙二酸(HOOC-COOH)俗名草酸,易溶于水,属于二元中强酸,生产和科学实验中有着广泛的用途。草酸晶体的组成可用H2C2O4・xH2O表示,为了测定x值,进行如下实验:称取Wg草酸晶体,配成100.00mL水溶液,量取25.00mL所配制的草酸溶液置于锥形瓶内,加入适量稀H2SO4后,用浓度为amol・L-1的KMnO4溶液滴定,
(1)将所发生的反应方程式完成并配平,将完整的化学方程式写在答题卡上。
 KMnO4 + H2C2O4?+ (?)---K2SO4 + CO2↑+ MnSO4 + (?) KMnO4 + H2C2O4?+ (?)---K2SO4 + CO2↑+ MnSO4 + (?)
(2)整个实验过程中不需要的仪器有?(填序号)。
a.托盘天平(带砝码,镊子)b.酸式滴定管? c.烧瓶
d.100mL容量瓶? e.烧杯? f.漏斗? g.锥形瓶
h.玻璃棒? i.药匙?
(3)实验中,标准KMnO4溶液应盛装在____式滴定管中。滴定终点时溶液的
颜色变化为?。
(4)在滴定过程中若用去amol・L-1的KMnO4溶液VmL,则所配制的草酸溶液的物质的量浓度为________mol・L-1,由此可计算x的值是___________。
(用含W、a、V的代数式表示)
(5)该小组同学将0.02mol草酸晶体(H2C2O4・2H2O)加入到100mL0.2mol/L的NaOH溶液中充分反应,测得反应后溶液呈酸性,则该溶液中各离子浓度由大到小的顺序为?
5、填空题 溶液配制及滴定:
(1)配制一定物质的量浓度的稀硫酸。
用24.5%硫酸(密度为 )配制100 mL 0.200 )配制100 mL 0.200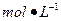 硫酸时,需用酸式滴定管量取24.5%硫酸_______ mL,洗净的酸式滴定管应先?,再用来量取所需的硫酸。 硫酸时,需用酸式滴定管量取24.5%硫酸_______ mL,洗净的酸式滴定管应先?,再用来量取所需的硫酸。
(2)用已配好的0.200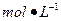 的硫酸溶液测定氢氧化钠样品中杂质氯化钠的含量。 的硫酸溶液测定氢氧化钠样品中杂质氯化钠的含量。
准确称取2.0克混有氯化钠的氢氧化钠固体试剂,将其配成100mL待测溶液,用浓度为0.200mol/L的标准硫酸酸溶液进行滴定,三次滴定的记录数据如下
实验编号
| 滴定开始时滴定管的读数为
| 滴定完成时,滴定管的读数为
| 待测溶液的体积
(mL)
| 1
| 0.07
| 22.59
| 20.00
| 2
| 0.22
| 22.72
| 20.00
| 3
| 0.35
| 22.83
| 20.00
|
测定出的氢氧化钠质量分数为 ?。
|