1������� ��10�֣�
��֪��ͼ��H����ɫҺ�壬�ų�����֮Դ��B�ǿ����к����������ʣ�E�Ǻ���ɫ���塣

��1��C�Ļ�ѧʽ��?��
��2��D��E���Ǵ�����Ⱦ����������ת���Ļ�ѧ����ʽ�ֱ��ǣ�
��D��E?��
��E��D?��
��3��E��H�ķ�Ӧ�У��������ͻ�ԭ������������?��
��4��C��F��Ӧ����G�Ļ�ѧ����ʽ��?��
�ο��𰸣���1��NH3
��2��D��E���Ǵ�����Ⱦ����������ת���Ļ�ѧ����ʽ�ֱ��ǣ�
��2NO��O2=2NO2
��3NO2��H2O=2HNO3��NO
��3��1��2
��4��HNO3��NH3=NH4NO3
�������������֮Դ����ɫҺ�壬��������Ϣ����ȷ��H��ˮ��A����������Ҳ������������BΪ�������ٸ���C���E�������ж��������μӷ�Ӧ����DΪһ��������EΪ����ɫ������������������ƶ�CӦ���ǰ�����Ҳ��AΪ����������E��H��Ӧ�õ�F����֪F�����ᡣ
��1��C�Ļ�ѧʽ����������ƶϿɵ�ΪNH3
��2��DΪNO��EΪNO2���ת���ķ��̣���2NO��O2=2NO2��3NO2��H2O=2HNO3��NO
��3����E��H���F�ķ�Ӧ�У�����������������������ԭ��Ӧ���������ͻ�ԭ���������Ⱦ��������ʵ���֮�ȣ�Ϊ1��2��
��4��HNO3��NH3=NH4NO3
�����Ѷȣ�һ��
2��ѡ���� 35.2g FeS��1000 mL 1.3mol/L������Һǡ����ȫ��Ӧ����Ӧ����������ΪFe2(SO4)3��Fe(NO3)3��������Ļ�ԭ����Ϊ��?��
A��N2
B��N2O
C��NO
D��NO2
�ο��𰸣�B
����������������,��֪0.4mol FeS��1.3 mol����ǡ����ȫ��Ӧ����Sԭ���غ����ɣ�0.4��3��mol��Fe2(SO4)3��Ȼ�������ԭ���غ㣬��֪���ɣ�0.4-0.8��3��mol��Fe(NO3)3����������Ե�����Ϊ3����0.4-0.8��3��=0.4mol���ٸ���Nԭ���غ㣬�ó����������Ե�����Ϊ1.3-0.4="0.9" mol.�����ݵ����غ���㣺0.4��9=0.9��4����֪����ԭ�ӻ��ϼ۽���4������N2O
�����Ѷȣ�һ��
3��ѡ���� ���������У���Ԫ�صĻ��ϼ���͵���
A��N2
B��NH3
C��NO
D��NO2
�ο��𰸣�B
�����������
�����Ѷȣ���
4������� ����ѧ��ѡ��2����ѧ�뼼����(15��)
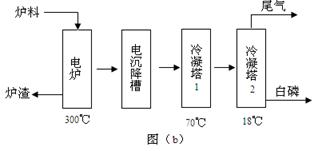
��ʯ��Ҫ������ơ�Ca3(PO4)2��H2O������ʯ��Ca3(OH)(PO4)3������ʽ���ڡ�ͼ(a)ΪĿǰ��������ʯ���õĴ������������ʪ��������ָ��ʯ�ù�������ֽ��Ʊ����ᡣͼ(b)���ȷ�������������������ʯ�Ƶ��������̡�
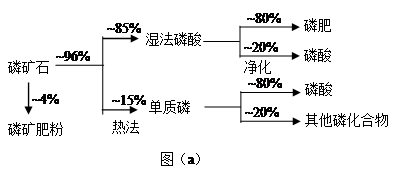
�������ʵ�����������£�
?
| �۵�/��
| �е�/��
| ��ע
|
����
| 44
| 280.5
| ?
|
PH3
| -133.8
| -87.8
| ������ˮ�����л�ԭ��
|
SiF4
| -90
| -86
| ��ˮ��
|
�ش��������⣺
��1����������ʯ����Ҫ����;�����������ϣ�Լռ��ʯʹ������? �G��
��2������ʯΪԭ�ϣ�ʪ�����������Ca3F(PO4)3��Ӧ�Ļ�ѧ����ʽΪ��?������1���ۺϺ�������������Լ30%����ʯ�������Ƶ�85�G����Ʒ����?�֡�
��3����ͼ(b)��ʾ���ȷ���������ĵ�һ���ǽ��������衢������̿����ʯ��ϣ����·�Ӧ���ɰ��ס�¯������Ҫ�ɷ��ǣ�?(�ѧʽ)������1����Ҫ�������ǣ�?������2����Ҫ�������ǣ�?
��4��β������Ҫ����?������������PH3��H2S��HF�ȣ���β����ͨ�봿����Һ���ɳ�ȥ?
��ͨ�����������Һ���ɳ�ȥ?(���ѧʽ)
��5�������ʪ�����ᣬ�ȷ����Ṥ�ո��ӣ��ܺĸߣ����ŵ��ǣ�??��
�ο��𰸣�(1)69; (2) Ca3F(PO4)3+5H2SO4=3H3PO4+ 5CaSO4+HF��;0.49����3��CaSiO3��Һ̬���ף���̬���ף���4��SiF4��CO��SiF4��HF�� H2S?��PH3?��5����Ʒ���ȴ�Ũ�ȴ�
���������(1)����ͼʾ��֪���������ϣ�Լռ��ʯʹ�����ı�����0.04+0.96��0.85��0.80="0.69." ��2������ʯΪԭ�ϣ��ù����������ܽ�Ca3F(PO4)3�����Ƶ����ᡣ���������غ㶨�ɿɵ÷�Ӧ�Ļ�ѧ����ʽΪCa3F(PO4)3+5H2SO4=3H3PO4+ 5CaSO4+HF��������P�غ�ɵù�ϵʽ P2O5��2H3PO4.142��P2O52����ȡ196�ݵ����ᡣ1���ۺϺ�������������Լ30%����ʯ������P2O5��������0.3�֣����Կ���ȡ85�G����Ʒ������������(196��0.3t)��142��0.85="0.49t;(3)" �������衢������̿����ʯ��ϣ��ڸ����·�Ӧ���˵õ������⣬�õ��������ԵĹ���������CaSiO3��������1���¶���70�棬280. 5��>t>44�����Դ�ʱ��Ҫ��������Һ̬���ף�������2���¶���12�棬���ڰ����۵㣬�ʴ�ʱ��Ҫ�������ǹ�̬���ס���4��������Ŀ�ṩ����Ϣ����Ϸ�Ӧʵ�ʣ���β������Ҫ����SiF4��CO������������PH3��H2S��HF�ȣ���β����ͨ�봿����Һ�� SiF4��HF�� H2S����̼���Ʒ�Ӧ����ȥ����ͨ�����������Һ�����ڴ���������ǿ�����ԣ���˿ɳ�ȥ�л�ԭ�Ե�PH3?����5�������ʪ�����ᣬ�ȷ����Ṥ�ո��ӣ��ܺĸߡ����Dz�Ʒ���ȴ������٣���������á�
�����Ѷȣ�һ��
5������� ��Ԫ�ؼ��仯�����ڹ�����ѧ��������������ҪӦ�á�
��1��д��ʵ������NH3�Ļ�ѧ��Ӧ����ʽ������������������������������?
��2����ҵ�ϳɰ���ԭ���ǵ����������������Ǵӿ����з�������ģ���������Դ��ˮ��̼�⻯���д������Ȼ��Ϊԭ����ȡ�����Ļ�ѧ��Ӧ����ʽ����������?������������������
��3���ںϳɰ���ԭ�����Ʊ������л���CO�Դ����ж������ã�����ȥԭ�����е�CO����ͨ�����·�Ӧ��ʵ�֣�CO(g)+H2O(g) CO2 (g)+ H2 (g) ��H��0����Ӧ�ﵽƽ���Ϊ���CO��ת���ʣ��ɲ�ȡ�Ĵ�ʩ������������?������֪1000Kʱ�÷�Ӧ��ƽ�ⳣ��K=0.627����ҪʹCO��ת���ʳ���90%������ʼ���У�c(H2O)�sc(CO)��������������������
CO2 (g)+ H2 (g) ��H��0����Ӧ�ﵽƽ���Ϊ���CO��ת���ʣ��ɲ�ȡ�Ĵ�ʩ������������?������֪1000Kʱ�÷�Ӧ��ƽ�ⳣ��K=0.627����ҪʹCO��ת���ʳ���90%������ʼ���У�c(H2O)�sc(CO)��������������������
��4�����ݻ�Ϊ2L�����з�����ӦCO(g)+H2O(g) CO2 (g)+ H2 (g)����֪c(CO)�뷴Ӧʱ��t�仯���ߢ�
CO2 (g)+ H2 (g)����֪c(CO)�뷴Ӧʱ��t�仯���ߢ�

����t0ʱ�̽����������������4L�����ڴ��ͼ�л��c(CO)�뷴Ӧʱ��t�仯���ߢ�

��5����ҵ������CO(NH2)2��CO2��NH3��һ�������ºϳɣ��仯ѧ��Ӧ����ʽΪ����������������
��6���ϳ�����ʱ������̼�� =4��CO2��ת������ʱ��ı仯��ϵ����ͼ��ʾ��
=4��CO2��ת������ʱ��ı仯��ϵ����ͼ��ʾ��
����A����淴Ӧ����v��(CO2)�� B�������Ӧ����Ϊv��(CO2)���������������������
����NH3��ƽ��ת����Ϊ������������ ��
�ο��𰸣���1��Ca(OH)2+2NH4Cl 2NH3��+CaCl2+2H2O
2NH3��+CaCl2+2H2O
��2�� CH4��H2O CO��3H2����CH4��2H2O
CO��3H2����CH4��2H2O ?CO2��4H2��
?CO2��4H2��
��3���ʵ������¶Ȼ����ճ�ȥ������̼?13.8?
��4��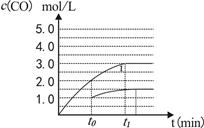
��5��
��6���١���?��30%
�����������1����ʵ����NH3�������������ȡ�ģ���ѧ��Ӧ����ʽΪ��Ca(OH)2+2NH4Cl 2NH3��+CaCl2+2H2O����2������Ȼ��Ϊԭ����ȡ�����Ļ�ѧ��Ӧ����ʽΪCH4��H2O
2NH3��+CaCl2+2H2O����2������Ȼ��Ϊԭ����ȡ�����Ļ�ѧ��Ӧ����ʽΪCH4��H2O CO��3H2����CH4��2H2O
CO��3H2����CH4��2H2O ?CO2��4H2����3����Ϊ�÷�Ӧ�Ǹ���Ӧǰ�����������ȵķ��ȷ�Ӧ����Ӧ�ﵽƽ���Ϊ���CO��ת���ʿ����ʵ������¶Ȼ����ճ�ȥ������̼������ˮ������Ũ�ȵȷ�������ƽ�������������м��㡣������ʼ���У�c(H2O)Ϊxmol/L,�ڷ�Ӧ������ CO��ת������СΪ90%����ת����CO����СֵΪ0.9xmol/L��?
?CO2��4H2����3����Ϊ�÷�Ӧ�Ǹ���Ӧǰ�����������ȵķ��ȷ�Ӧ����Ӧ�ﵽƽ���Ϊ���CO��ת���ʿ����ʵ������¶Ȼ����ճ�ȥ������̼������ˮ������Ũ�ȵȷ�������ƽ�������������м��㡣������ʼ���У�c(H2O)Ϊxmol/L,�ڷ�Ӧ������ CO��ת������СΪ90%����ת����CO����СֵΪ0.9xmol/L��?
CO��g��+ H2O��g��? CO2��g��+? H2��g��
��ʼŨ��(mol/L)? x? y? 0? 0
�仯Ũ��(mol/L)? 0.9x? 0.9x? 0.9x? 0.9x
ƽ��Ũ��(mol/L)? 0.1x? y-0.9x? 0.9x? 0.9x��
����ƽ�ⳣ����ʽ�� ;���
;��� ���ֻҪ���ߵı�ֵ����13.8��ת���ʾͻᳬ��90%����4�����������ݻ���2L��Ϊ4Lʱ����Ӧ���������ʵ�Ũ�ȶ���ԭ����һ�룬Ũ�ȼ�С����Ӧ���ʼ������ﵽƽ������Ҫ��ʱ���ӳ������ڸ÷�Ӧ�Ƿ�Ӧǰ�����������ȵķ�Ӧ�����Լ�Сѹǿ����ѧƽ�ⲻ�����ƶ����ݻ���ԭ����2������ﵽƽ��ʱ�����ʵ�Ũ�ȶ���ԭƽ���1/2.��ͼΪ��
���ֻҪ���ߵı�ֵ����13.8��ת���ʾͻᳬ��90%����4�����������ݻ���2L��Ϊ4Lʱ����Ӧ���������ʵ�Ũ�ȶ���ԭ����һ�룬Ũ�ȼ�С����Ӧ���ʼ������ﵽƽ������Ҫ��ʱ���ӳ������ڸ÷�Ӧ�Ƿ�Ӧǰ�����������ȵķ�Ӧ�����Լ�Сѹǿ����ѧƽ�ⲻ�����ƶ����ݻ���ԭ����2������ﵽƽ��ʱ�����ʵ�Ũ�ȶ���ԭƽ���1/2.��ͼΪ��

��5����ҵ������CO(NH2)2��CO2��NH3��һ�������ºϳɣ��仯ѧ��Ӧ����ʽΪ ��6������Ϊ��B��ʱ��Ӧ�ﵽƽ�⣬��A�㻹û�дﵽƽ�⡣��Ӧ�Ǵ���?��Ӧ����ʼ�ġ��ڴﵽƽ��ǰ���κ�ʱ�̣������κ�����V��������V�档����A����淴Ӧ����v��(CO2) ��B�������Ӧ����Ϊv��(CO2)�����ڼ��跴Ӧ��ʼʱc(CO2)=1mol/L,��c(NH3)=4mol/L.���ﵽƽ��ʱ����CO2��ת����Ϊ60%.ת��Ũ��Ϊ: 1mol/L��60%=0.6mol/L.���ݷ���ʽ��֪NH3ת��Ũ��Ϊ1.2mol/L���NH3��ƽ��ת����Ϊ(1.2mol/L��4mol/L) ��100%=30%.
��6������Ϊ��B��ʱ��Ӧ�ﵽƽ�⣬��A�㻹û�дﵽƽ�⡣��Ӧ�Ǵ���?��Ӧ����ʼ�ġ��ڴﵽƽ��ǰ���κ�ʱ�̣������κ�����V��������V�档����A����淴Ӧ����v��(CO2) ��B�������Ӧ����Ϊv��(CO2)�����ڼ��跴Ӧ��ʼʱc(CO2)=1mol/L,��c(NH3)=4mol/L.���ﵽƽ��ʱ����CO2��ת����Ϊ60%.ת��Ũ��Ϊ: 1mol/L��60%=0.6mol/L.���ݷ���ʽ��֪NH3ת��Ũ��Ϊ1.2mol/L���NH3��ƽ��ת����Ϊ(1.2mol/L��4mol/L) ��100%=30%.
�����Ѷȣ�����