1、选择题 下列所用除杂的试剂和操作方法均正确的是
A.②④
B.①④
C.②③
D.①③
参考答案:A
本题解析:试题分析:乙烯中含有碳碳双键,也能和氯水发生加成反应,①不正确,应该用氢氧化钠溶液;乙酸乙酯不溶于饱和碳酸钠溶液中,而乙酸可以溶解在饱和碳酸钠溶液中,所以②正确;苯酚虽然能和溴水反应,但生成的白色沉淀又可以溶解在苯中,③不正确,应该用氢氧化钠溶液;乙醇和水互溶,所以应该用新制的生石灰,蒸馏,④正确,答案选A。
考点:考查物质的分离和提纯
点评:该题是高考中的重要考点之一,也是高考中的常见题型,属于中等难度的试题。该题需要明确的是在解答物质分离提纯试题时,选择试剂和实验操作方法应遵循三个原则: 1.不能引入新的杂质(水除外),即分离提纯后的物质应是纯净物(或纯净的溶液),不能有其他物质混入其中;2.分离提纯后的物质状态不变;3.实验过程和操作方法简单易行,即选择分离提纯方法应遵循先物理后化学,先简单后复杂的原则。
本题难度:简单
2、选择题 0.2L?1mol?L-1的FeCl3与0.1L?2mol?L-1的KCl溶液中,Cl-的物质的量浓度之比为
A.1:2
B.3:1
C.3:2
D.1:1
参考答案:C
本题解析:分析:先根据溶液中氯离子的物质的量浓度=盐的浓度×化学式中氯离子个数,求出各溶液中Cl-的物质的量浓度,然后求比值.
解答:0.2L?1mol?L-1的FeCl3溶液中Cl-的物质的量浓度为1mol?L-1×3=3mol?L-1,0.1L?2mol?L-1的KCl溶液中Cl-的物质的量浓度为2mol?L-1,Cl-的物质的量浓度之比为3:2,故选:C.
点评:本题考查了溶液中氯离子物质的量浓度的计算,溶液中氯离子的物质的量浓度为盐的浓度与化学式中离子个数的积,与溶液的体积无关.
本题难度:困难
3、选择题 下列物质与水混合后静置,不会出现分层的是( )
A.汽油
B.苯
C.四氯化碳
D.乙醇
参考答案:A.汽油和水互不相溶,与水混合后静置,出现分层,故A不选;
B.苯和水互不相溶,与水混合后静置,出现分层,故B不选;
C.四氯化碳水互不相溶,与水混合后静置,出现分层,故C不选;
D.乙醇与水混溶,不分层,故D选.
故选D.
本题解析:
本题难度:一般
4、简答题 1,5-二硝基萘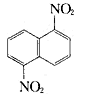 和1,8-二硝基萘
和1,8-二硝基萘 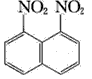 中,后者可溶于质量分数大于98% 的浓硫酸,而前者不能。简述如何将这两种异构体的混合物分离?
中,后者可溶于质量分数大于98% 的浓硫酸,而前者不能。简述如何将这两种异构体的混合物分离?
参考答案:①在混合物中加入足量的质量分数大于98%的浓硫酸.充分搅拌;
②用耐酸漏斗过滤出不溶物,分离出滤液;
③将滤液沿烧杯内 壁加入适量水中,充分搅拌,出现沉淀;
④将上述悬浊液用耐酸漏 斗过滤.得到固体1,8-二硝基萘;
⑤用蒸馏水冲洗滤纸上的固体 若十次,直至洗净。
本题解析:
本题难度:一般
5、选择题 用括号中的试剂除去各组中的杂质,不正确的是( )
A.苯中的甲苯(溴水)
B.乙醇中的水(新制CaO)
C.乙醛中的乙酸(NaOH)
D.乙酸乙酯中的乙酸(饱和Na2CO3溶液)
参考答案:A.苯和甲苯都不与溴反应,且都可溶解溴,故A错误;
B.水可与氧化钙反应生成氢氧化钙,除去乙醇中的水,可加入CaO,然后用蒸馏的方法分离,故B正确;
C.乙酸能与氢氧化钠溶液反应而乙醛不能,然后用蒸馏即可分离,故C正确;
D.乙酸乙酯难溶于饱和碳酸钠溶液,但乙酸和碳酸钠反应,则除去乙酸乙酯中的乙酸,可用饱和碳酸钠溶液,然后用分液的方法分离,故D正确.
故选A.
本题解析:
本题难度:简单