1、选择题 海水是宝贵的化学资源,可以从海水中提取的物质有
A.Si
B.Br2
C.Na
D.Cl2
参考答案:BCD
本题解析:可以从海水中提取的物质有单质溴、氯气和金属钠,但得不到单质硅,答案选BCD。
点评:该题是基础性试题的考查,难度不大,记住即可。有助于调动学生的学习兴趣和学习积极性,激发学生的求知欲。
本题难度:简单
2、填空题 (7分)海水是人类宝贵的自然资源,从海水中可以提取多种化工原料。下图是某工厂对海水资源综合利用的示意图。
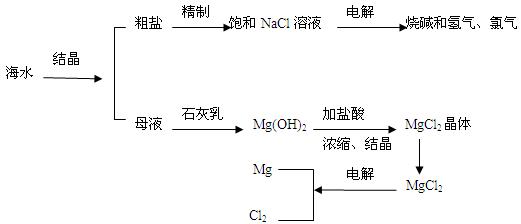
(1)粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制后可得NaCl饱和溶液。精制时通常向精盐溶液中依次加入过量的BaCl2溶液,过量的NaOH溶液和过量的Na2CO3溶液,过滤出沉淀后再向滤液加入盐酸至溶液呈中性。请写出下列操作中有关化学反应的离子方程式:
①向溶液中加入过量的Na2CO3溶液:__________________、_____________________;
②电解氯化钠溶液:______________________________________________。
(2)母液中含有K+、Na+、Mg2+等阳离子,从图中可以看出,对母液进行一系列的加工可制得金属镁。
①从离子反应的角度思考,在母液中加入石灰乳所起的作用是:(用离子反应方程式回答)___________________________。
②简述怎样操作才能由氯化镁晶体得到无水氯化镁:____________________________。
参考答案:(7分)
(1)?①Ba2+ + CO32-="=" BaCO3↓、? Ca2+ + CO32-="=" CaCO3↓(共2分)
②2Cl-+2H2O 2OH-+H2↑+Cl2↑(2分)
2OH-+H2↑+Cl2↑(2分)
(2) ①Ca(OH)2+Mg2+==Mg(OH)2+Ca2+? (2分)
②?在HCl气体氛围下加热? (1分)
本题解析:略
本题难度:一般
3、实验题 (8分)从海水中可以获得淡水、食盐,并可提取镁和溴等物质。
(一)海水淡化的方法主要有?(填一种)
(二)从海水中提取溴和镁的流程如下图所示:
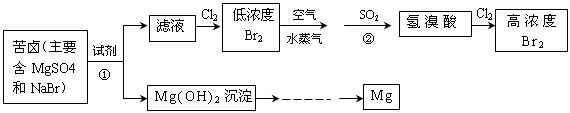
(1)提取Br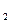 时第一次通入Cl
时第一次通入Cl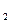 后发生反应的离子方程式是?;②中表现
后发生反应的离子方程式是?;②中表现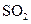 表现?(填“氧化”或“还原”)性;
表现?(填“氧化”或“还原”)性;
第二次通入Cl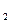 后,要提取Br
后,要提取Br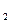 还要进行的操作为?。
还要进行的操作为?。
(2)为了实现对镁离子的富集,①中加入的足量试剂是?(填化学式);
试从节约能源,提高金属镁的纯度分析,以下最适宜的冶炼的方法是?(填字母)。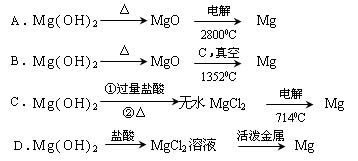
参考答案:(8分)
(一)蒸馏法(1分,其他合理答案均给分)
(二)(1)Cl2 + 2Br-= 2Cl- + Br2 (2分);还原(1分);萃取、分液(2分)
(2)Ca(OH)2(或NaOH等其它合理答案均给分)(1分);C (1分)
本题解析:略
本题难度:简单
4、选择题 下列物质中,不属于合金的是
[? ]
A.硬铝
B.水银
C.黄铜
D.钢铁
参考答案:B
本题解析:
本题难度:简单
5、选择题 铝镁合金因坚硬、轻巧、美观、洁净、易于加工而成为新型建筑装潢材料,主要用于制作窗框、卷帘门、防护栏等。下列与这些用途无关的性质是
[? ]
A.不易生锈
B.导电性好
C.密度小
D.强度高
参考答案:B
本题解析:
本题难度:简单