1、选择题 日本9级大地震导致的福岛核泄漏,主要泄露的物质为碘131,碘131一旦被人体吸入会引发甲状腺疾病,引发低甲状腺素(简称低甲)症状,患者必须长期服用甲状腺素片,而更严重的甚至可能引发甲状腺癌变.下列说法中不正确的是( )
A.131I和127I互为同位素
B.碘处于第五周期ⅦA族
C.干燥的氯气接触淀粉KI试纸,试纸变蓝
D.碘的CCl4溶液呈红色
参考答案:A、131I和127I的质子数相同,都为53,但中子数不同,分别为78和74,故二者属于同位素,故A正确;
B、碘的原子序数为53,在元素周期表中第五周期ⅦA族,故B正确;
C、氯气与KI的反应属于离子反应,应在溶液中进行,干燥的氯气和KI不反应,故C错误;
D、碘的CCl4溶液中,如浓度较大呈紫色,浓度较小呈红色,故D正确.
故选C.
本题解析:
本题难度:简单
2、选择题 X、Y均为元素周期表中前20号元素,其简单离子的电子层结构相同,下列说法正确的是?
[? ]
A.由mXa+与nYb-得,m+a=n-b?
B.X2-的还原性一定大于Y-
C.X、Y一定不是同周期元素
D.若X的原子半径大于Y,则气态氢化物的稳定性HmX一定大于HnY
参考答案:B
本题解析:
本题难度:简单
3、选择题 X、Y、Z、W四种短周期元素的最外层电子数之和为20.在周期表中X与Y、Z、W紧密相邻,X、Y两元素的原子序数之和等于Z元素的原子序数.下列说法正确的是( )
A.原子序数:Z>Y>X>W
B.X、Y、Z、W形成的单质最多有6种
C.X元素最高价氧化物对应水化物的化学式为:H3XO4
D.四种元素的气态氢化物中,W的气态氢化物最稳定
参考答案:A、W是C元素,X是N元素,Y是O元素,Z是P元素,所以原子序数Z>Y>X>W,故A正确.
B、碳元素形成的单质有金刚石、石墨、C60等,氮元素形成的单质有氮气,氧元素形成的单质有氧气和臭氧,磷元素形成的单质有红磷和白磷,故B错误.
C、X是N元素,X元素最高价氧化物对应水化物是硝酸,其化学式为:HNO3,故C错误.
D、非金属性越强的非金属元素其气态氢化物越稳定,这四种元素中非金属性最强的是O元素,所以氢化物最稳定的是Y,故D错误.
故选A.
本题解析:
本题难度:一般
4、选择题 短周期元素W、X、Y和Z的原子序数依次增大。W原子形成的单质是密度最小的气体,X原子的最外层电子数是内层电子数的2倍,Y原子的最外层电子数是其电子层数的3倍,元素Z是地壳中含量最多的金属元素。下列说法不正确的是
[? ]
A.元素X与W形成的原子个数比为1:1的化合物有多种
B.Y与Z的简单离子的半径大小是Yn-<Zm+
C.元素Z的单质与氢氧化钠溶液或盐酸反应均有氢气生成
D.元素Y可与元素X形成直线型化合物XY2
参考答案:B
本题解析:
本题难度:一般
5、简答题 Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大,Q是周期表中原子半径最小的元素,Q与W组成的化合物是一种温室气体,W与Y、X与Y组成的化合物是机动车排出的大气污染物,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物.
(1)W在元素周期表中的位置是______,Z2Y的电子式是______.
(2)①已知“凡气体分子总数增多的反应一定是熵增大的反应”.根据所学知识判断如下反应2WY(g)=2W(s)+Y2(g)△H>0,在常温下______自发进行(填“能”或“不能”).
②400℃时,在0.5L的反应容器中用X2、Q2反应合成XQ3反应,达到平衡时,测得X2、Q2、XQ3的物质的量分别为2mol、1mol、2mol,则此反应在400℃时的化学平衡常数为______
(3)2.24L(标准状况)XQ3被200mL?1mol/L?QXY3溶液吸收后,所得溶液中离子浓度从大到小的顺序是______.
(4)WQ4Y与Y2的反应可将化学能转化为电能,其工作原理如图所示,a极的电极反应式是______
(5)X和Z组成的一种离子化合物,能与水反应生成两种碱,该反应的化学方程式是______.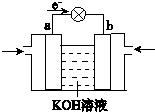
参考答案:Q是周期表中原子半径最小的元素,应为H,Q与W组成的化合物是一种温室气体,该气体为CH4,则W为C,W与Y、X与Y组成的化合物是机动车排出的大气污染物,为CO和NOx,则Y为O,X为N,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物,这两种离子化合物分别为Na2O、Na2O2,作为Z为Na,则
(1)W为C,原子序数为6,原子核外有2个电子层,最外层电子数为6,应位于周期表第二周期IVA族,
Z2Y为Na2O,为离子化合物,电子式为
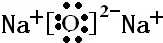
,
故答案为:第二周期IVA族;
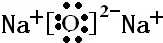
;?
(2)①由自由能判据△G=△H-T?△S,可知当△H<T?△S时反应才能自发进行,即必须在较高的温度下才可以进行,化学反应能否自发进行取决于焓变和熵变的综合判据,不能只由焓变或熵变来决定,故答案为:不能;
?②达平衡时,各物质的浓度分别为:c(N2)=4mol/L,c(H2)=2mol/L,c(NH3)=4mol/L,
则k=c2(NH3)c(N2)×c3(H2?)=424×23=0.5,故答案为:0.5;
(3)n(NH3)=2.24L22.4L/mol=0.1mol,n(HNO3)=0.2L×1mol/L=0.2mol,HNO3过量,生成NH4NO3,二者物质的量相等,但由于NH4+水解,则c(H+)>c(NH4+),所以溶液中存在c(NO3-)>c(H+)>c(NH4+)>c(OH-),
故答案为:c(NO3-)>c(H+)>c(NH4+)>c(OH-);?
(4)CH3OH碱性燃料电池中,CH3OH为电池的负极反应,被氧化,电极反应式为CH3OH+8OH--6e-=CO32-+6H2O,
故答案为:CH3OH+8OH--6e-=CO32-+6H2O;
(5)X和Z组成的一种离子化合物为Na3N,能与水反应生成两种碱,生成物为NaOH和NH3?H2O,反应的化学方程式为Na3N+4H2O=3NaOH+NH3?H2O,
故答案为:Na3N+4H2O=3NaOH+NH3?H2O.
本题解析:
本题难度:一般