1��ѡ���� �����������������ȷ���ǣ�������
A��������ʹʪ�ĺ첼����ɫ��������������Ư����
B������û��Ư���ԣ���ͨ��Ʒ����Һ�У�Ʒ����ɫ
C���������Ժ��κν���ֱ�ӻ���
D�������ж���������ζʱҪС�Ľ�����ƿ���ڱǿ���ֱ��������ζ
�ο��𰸣�A������������������Ư���ԣ���������ʹʪ�ĺ첼����ɫ�����������õ���������ˮ��Ӧ���ɵĴ����ᣬ��A����
B����������ˮ��Ӧ���ɵĴ����ᣬ���������Ư���ԣ���ͨ��Ʒ����Һ�п���ʹ֮��ɫ����B��ȷ��
C����ͨ������£�����������ý������ϻ��ý���������Ӧ���뼫�����ý�������Ӧ����C����
D��������ʱ������ֱ�ӷ��ڱ������ţ�Ӧ�����ڼ���ƿ�������ȶ������������ζ����D����
��ѡ��B��
���������
�����Ѷȣ�һ��
2��ѡ���� ����˵����ȷ���ǣ���������
A����ʢŨ������Լ�ƿ�ɿ�����ɫ��������˵��HCl���ȶ�
B�������е���Ũ���ᣬ���DZ�ڣ���˵��Ũ��������������
C�����������е���Ũ���ᣬ��������ɫ��Ϊ��ɫ����˵��Ũ��������ˮ��
D��̼�ᡢ������ʹ����ᶼ�Dz��ȶ�����
�ο��𰸣�D
�����������ʢŨ������Լ�ƿ�ɿ�����ɫ��������˵��Ũ����е�ͣ��ӷ������������һ���������ʣ���HCl���ȶ����أ���A����Ũ����ʹ���DZ��������������ˮ�ԣ�B����Ũ����ʹ����������������������ˮ�ԣ�C����̼�ᡢ������ʹ����᳣���¶��ֽ⣬���Dz��ȶ����ᣬD��ȷ��
�����Ѷȣ�һ��
3������� ���Ƶ���ˮ��______ɫ��������Ϊ��ˮ����______���ӣ��������ţ����ڣ�����ˮ�е��뼸��AgNO3��Һ���۲쵽��������______��˵����ˮ����______���������ţ����ڣ���ɫʯ����ֽ������ˮ�����ȱ�죬�úܿ�����ɫ��������Ϊ______��ˮ�����պ���ɫ����ʧ�����ų����壬�÷�Ӧ��ѧ����ʽ��______��
�ο��𰸣�������ˮ�д���Cl2+H2O?H++Cl-+HClO��������������ˮ�����Ƶ���ˮ�Ի���ɫ��������Ϊ��ˮ����Cl2���ӣ�����Cl-������ˮ�е��뼸��AgNO3��Һ���۲쵽���������а�ɫ�������ɣ���Һ�����ԣ���ʹʯ���죬��ͬʱ����ǿ�����ԵĴ����ᣬ������ʯ���ɹ۲쵽��ɫʯ����ֽ������ˮ�����ȱ�죬�úܿ�����ɫ������ʱ�������ᷢ��2HClO��.2HCl+O2���ɹ۲쵽����ɫ����ʧ�����ų����壬
�ʴ�Ϊ�����̣�Cl2���а�ɫ�������ɣ�Cl-����ˮ�д���H+�����ԣ����ʹ��ֽ��죬��ͬʱ����HClO���ӣ�HClO����ǿ�����ԣ�ʹ��ɫ������ɫ�������ɫ�漴��ʧ��2HClO��.2HCl+O2��
���������
�����Ѷȣ�һ��
4������� ���ӻ�����AB2�����������ӵĵ��Ӳ�ṹ��ͬ��1 mol AB2�к�54 mol���ӣ��������з�Ӧ��
��H2��B2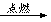 C
C
��B2��X��Y��AB2��H2O
��Y��C��AB2��Z��Z��Ư�����á�
�������������ش��������⣺
��1��д���������ʵĻ�ѧʽ��AB2__________��X________��Y________��Z________��
��2���õ���ʽ��ʾAB2���γɹ��̣�_____________________________________________��
��3��д����Ӧ�ڵĻ�ѧ����ʽ��______________________________________��
�ο��𰸣���1��CaCl2��Ca��OH��2��Ca��ClO��2��HClO
��2��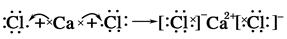
��3��2Cl2��2Ca��OH��2=CaCl2��Ca��ClO��2��2H2O
�������������Ŀ��Ϣ��֪�������ӻ�������A2����B�������������Ϊ18������Ԫ��A��B�ֱ���Ca��Cl��
���ɻ�ѧ��Ӧ��H2��Cl2�D��C���Ƴ�CΪHCl����Ϊ��Ӧ�ڣ�Cl2��X�D��Y��CaCl2��H2O������֪X�к���Ԫ��Ca��H��O����X������Ca��OH��2����Ӧ��Ϊ��2Cl2��2Ca��OH��2=CaCl2��Ca��ClO��2��2H2O�����Ӧ��Ϊ��Ca��ClO��2��2HCl=CaCl2��2HClO��
�����Ѷȣ�һ��
5��ʵ���� ��ˮFeCl3���غ�ɫ�����׳��⣬100������ʱ��������ҵ�ϳ������л��ϳɴ�����ʵ���ҿ�������װ��(�г�������ȥ)�Ʊ����ռ���ˮFeCl3��
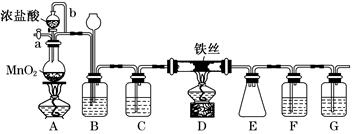
��ش�
(1)װ��A�з�Ӧ�����ӷ���ʽΪ__________________________________________��
(2)װ��F�����ӵ��Լ�Ϊ_________________________________________________��
(3)����b������Ϊ_____________________________________________________��
װ��B������Ϊ________________________________________________________��
(4)ʵ��ʱӦ�ȵ�ȼA���ľƾ��ƣ���Ӧһ������ٵ�ȼD���ľƾ��ƣ�ԭ��Ϊ_______________________________________________________��
(5)��Ӧ������жװ��ǰ��������еIJ�����_________________________________
(6)Ϊ�������ò�Ʒ���Ƿ���FeCl2���ɽ�������ʵ�飺ȡE���ռ��IJ�����������ˮ�ܽ⣬��������Һ�м���һ���Լ������Լ�Ϊ________(�����)��
��Fe�ۡ���KSCN��Һ��������KMnO4��Һ����NaOH��Һ
�ο��𰸣�(1)MnO2��4H����2Cl��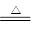 Mn2����Cl2����2H2O��(2)Ũ�����ŨH2SO4��(3)ƽ��ѹǿ(��ʹŨ����˳������)����ȥCl2�е�HCl���壬�ж�ʵ������е����Ƿ�Ʒ������(4)�ž�ʵ��װ���еĿ���
Mn2����Cl2����2H2O��(2)Ũ�����ŨH2SO4��(3)ƽ��ѹǿ(��ʹŨ����˳������)����ȥCl2�е�HCl���壬�ж�ʵ������е����Ƿ�Ʒ������(4)�ž�ʵ��װ���еĿ���
(5)����a��ͨ��������ų�װ���ڲ�����Cl2����֤���ո�����(���������𰸾���)��(6)��
���������(1)MnO2��Ũ���ᷴӦ�����ӷ���ʽΪMnO2��4H����2Cl��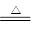 Mn2����Cl2����2H2O��(2)Fװ�����ڷ�ֹ����ˮ�⣬����F��ʢ��Ũ���ᡣ(3)����b��������ƽ��ѹǿ��ʹŨ����˳�����£�װ��B�������dz�ȥCl2�е�HCl���壬ͬʱ�ж�ʵ������е����Ƿ�Ʒ������(4)װ���еĿ�����Ӱ���Ʒ�Ĵ��ȣ����Ե�ȼD���ľƾ���ǰ�����ž�ʵ��װ���еĿ�����(5)�����ж����ڲ�жװ��ǰ���뱻��ȫ���ա�(6)�������Ը��������Һ�����������ӡ�
Mn2����Cl2����2H2O��(2)Fװ�����ڷ�ֹ����ˮ�⣬����F��ʢ��Ũ���ᡣ(3)����b��������ƽ��ѹǿ��ʹŨ����˳�����£�װ��B�������dz�ȥCl2�е�HCl���壬ͬʱ�ж�ʵ������е����Ƿ�Ʒ������(4)װ���еĿ�����Ӱ���Ʒ�Ĵ��ȣ����Ե�ȼD���ľƾ���ǰ�����ž�ʵ��װ���еĿ�����(5)�����ж����ڲ�жװ��ǰ���뱻��ȫ���ա�(6)�������Ը��������Һ�����������ӡ�
�����Ѷȣ�һ��