1、选择题 燃烧法是有机化学发展初期测定简单有机物组成的常用方法。验证某有机物是否为含氧元素,应完成的实验内容是

A.只有验证它完全燃烧后产物只有H2O和CO2
B.只有测定其燃烧产物中H2O和CO2物质的量的比值
C.测定完全燃烧时消耗有机物与生成的CO2、H2O的物质的量之比
D.测定该试样完全燃烧后生成CO2和H2O以及消耗O2三者的物质的量之比
参考答案:D
本题解析:考查有机物分子式的判断。产物是CO2和水不能说明是否含有氧元素,A不正确。B中只能得出有机物中碳、氢原子的个数之比。C中只能得出有机物中含有的碳原子和氢原子的个数,所以正确的做法是选项D,根据氧原子守恒即可判断是否含有氧元素。答案选D。
本题难度:简单
2、填空题 (6分)(1)标准状况下,2.24LCH4、HCHO、C2H6的混合气充分燃烧后,生成CO2 0.14mol,该混合气体中C2H6的体积分数??
(2)某气态不饱和烃在标准状况下的密度为2.41g/ L。取0.54 g该烃恰好与浓度为0.2 mol / L的溴水100mL完全反应,使溴水完全褪色。求该烃的分子式及结构简式
参考答案:
25、(6分)40%
∴分子式为C4H6 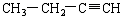 ?
?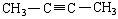 ?
?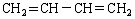
本题解析:(1)设CH4、HCHO、C2H6的物质的量分别为a、b、c,则有
a + b + c =0.1
a + b + 2c =0.14
解得c =" 0.04mol" ,故该混合气体中C2H6的体积分数 w =" 0.04/0.1" × 100% =" 40%" 。
(2)气态不饱和烃在标准状况下的密度为2.41g/ L,则其摩尔质量为 2.41g/ L × 22.4L =" 54" g 。由题意可知0.01mol该烃恰好与0.02mol溴水完全反应,则1mol该烃可能含有2mol碳碳双键,也可能含有1mol碳碳三键,因此该烃符合通式CnH2n-2 ,故有 12n +(2n-2)=" 54" ,解得n="4" 。因此,该烃的分子式为C4H6,结构简式有 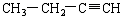 ?,
?,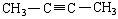 ,
,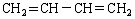 。
。
点评:本大题(1)考查了根据混合气体的体积及燃烧后CO2气体的物质的量,计算气体的体积分数,相对来说比较简单,只要根据物质守恒来计算即可。(2)考查了基本官能团的推断,并根据其密度计算烃的分子量,推断出烃的分子式,并写出其结构简式。只要会推断官能团,其他的问题都不难解决。
本题难度:一般
3、选择题 1995年美国化学家首先制得了碳的第四种同素异形体,链式炔碳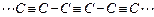 该物质一个分子中含300~500个碳原子。2001年美日两国化学家又联合制得了导电塑料聚乙炔-[CH="CH]-" n。有关这两种物质的下列说法正确的是
该物质一个分子中含300~500个碳原子。2001年美日两国化学家又联合制得了导电塑料聚乙炔-[CH="CH]-" n。有关这两种物质的下列说法正确的是
A.都是有机高分子化合物
B.都可以看作为乙炔的加聚产物
C.都能燃烧且一定条件下都可以与H2发生加成反应
D.都有很高的熔点和硬度且难溶于水
参考答案:C
本题解析:略
本题难度:一般
4、计算题 某含氧有机物,它的相对分子质量为74。7.4 g该含氧有机物充分燃烧后的产物通过浓硫酸后增重5.4 g,通过足量澄清石灰水后有30 g白色沉淀生成。求:
(1)该含氧有机物的分子式;
(2)该含氧有机物有多种同分异构体,写出其中能水解的同分异构体的结构简式。
参考答案:(1)C3H6O2
(2)HCOOCH2CH3? CH3COOCH3
本题解析:(1)据题意可知:
n(C)=n(CO2)=n(CaCO3)= =0.3 mol,
=0.3 mol,
n(H)=2n(H2O)=2× =0.6 mol
=0.6 mol
n(O)=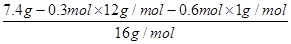 =0.2 mol。
=0.2 mol。
则有机物的实验式为C3H6O2,因其相对分子质量为74,则其分子式为C3H6O2。
(2)若该含氧有机物能水解,则含有 官能团。
官能团。
本题难度:一般
5、选择题 下列各组混合物总物质的量不变时,各组分以任意比混合后充分燃烧消耗O2的量不变的是(?)
A.乙烯、乙醇、乙醛
B.乙炔、乙醛、乙二醇?
C.甲醇、甲醚、甲醛?
D.乙烷、甘油、乙醇
参考答案:B
本题解析:根据有机物的燃烧CnHmOz+ 02=nCO2+
02=nCO2+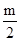 H2O通式可知,早物质的量相等的条件下,有机物完全燃烧消耗氧气的物质的量只与
H2O通式可知,早物质的量相等的条件下,有机物完全燃烧消耗氧气的物质的量只与 有关系,所以根据有机物的化学式可知,选项B正确。即在碳原子个数相等的条件下,每增加2个氢原子,分子中就增加1个氧原子。或者在氢原子个数相等的条件下,分子中每增加1个碳原子,就增加2个氧原子,答案选B。
有关系,所以根据有机物的化学式可知,选项B正确。即在碳原子个数相等的条件下,每增加2个氢原子,分子中就增加1个氧原子。或者在氢原子个数相等的条件下,分子中每增加1个碳原子,就增加2个氧原子,答案选B。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生能力的培养和解题方法的指导与训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的应试能力和逻辑推理能力。该题的关键是利用好燃烧通式,总结出规律。
本题难度:一般