1、选择题 将0.1 mol某有机物与0.3 mol O2混合,于密闭反应器中用电火花点燃,将燃烧产物通入过量的澄清石灰水中,可得到沉淀20g,溶液质量减少5.8g;剩余气体继续通过灼热的CuO,可以使CuO质量减少1.6g,由此可知该有机物的分子式为(?)
A.C2H6O
B.C3H6O
C.C3H6O2
D.C4H8O2
参考答案:C
本题解析:将燃烧产物通入过量的澄清石灰水中,可得到沉淀20g为生成碳酸钙的质量,其物质的量为 =0.2mo1,根据碳原子守恒生成二氧化碳的物质的量为0.2mol,该有机物的燃烧产物可以与CuO反应,说明有CO生成,可以使CuO质量减少1.6g,则:
=0.2mo1,根据碳原子守恒生成二氧化碳的物质的量为0.2mol,该有机物的燃烧产物可以与CuO反应,说明有CO生成,可以使CuO质量减少1.6g,则:
CuO+CO Cu+CO2,质量减少
Cu+CO2,质量减少
1mol? 16g
n(CO)? 1.6g
则n(CO)=0.1mol,
故0.1mol有机物含有C原子为0.2mol+0.1mol=0.3mol,溶液质量减少5.8g,则生成的碳酸钙与燃烧生成的水、二氧化碳的质量之差为5.8g,故燃烧生成水的质量为20g-0.2mol×44g/mol-5.8g=5.4g,故燃烧生成水的物质的量为 =0.3mol,则0.1mol有机物含有H原子为0.3mol×2=0.6mol,根据氧原子守恒可知,0.1mol有机物含有O原子的物质的量为0.2mol×2+0.1mol+0.3mol-0.3mol×2=0.2mol,故有机物分子中N(C)=
=0.3mol,则0.1mol有机物含有H原子为0.3mol×2=0.6mol,根据氧原子守恒可知,0.1mol有机物含有O原子的物质的量为0.2mol×2+0.1mol+0.3mol-0.3mol×2=0.2mol,故有机物分子中N(C)= =3、N(H)=
=3、N(H)=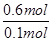 =6、N(O)=
=6、N(O)= =2,故有机物的分子式为C3H6O2。
=2,故有机物的分子式为C3H6O2。
本题难度:一般
2、选择题 等物质的量的下列物质,与足量氢气发生加成反应消耗氢气最多的是(?)
A.
B.
C.
D.
参考答案:C
本题解析:发生加成反应时1 mol苯环消耗3 mol H2,而D项中相当于两个苯环并在一起共用两个碳原子,1 mol该物质发生加成反应时消耗5 mol H2,而C中有两个苯环,发生加成反应共需6 mol H2,故C消耗的氢气最多。
本题难度:一般
3、选择题 取0.2mol两种气态烃组成的混合气,其质量为3.5g, 则下列说法正确的是?( )
A.一定有乙烯
B.一定有甲烷
C.一定没有甲烷
D.一定有乙烷
参考答案:B
本题解析:混合气体的平均摩尔质量为M(平均)= 3.5g÷0.2mol=17. 5g/mol.说明一种气体的相等分子质量比17. 5大,一种气体的相等分子质量比17. 5小。而相对分子质量比17. 5小的只有CH4的16,故选项为B。
本题难度:一般
4、填空题 某校化学探究小组探究有机化合物A的结构简式,其基本过程如下:
(1)取4.2g该有机化合物燃烧,将燃烧产物依次通入浓硫酸、足量澄清石灰水溶液,实验后,浓硫酸增重1.8g,生成碳酸钙的质量为20g,由此可确定A的最简式为_________。
(2)由质谱分析测定出A的相对分子质量为84,由此可确定A的分子式为_________。
(3)取8.4gA和足量银氨溶液反应,最终生成43.2g银,由此可确定A的结构简式为_____。
参考答案:(1)C2H2O;(2)C4H4O2;(3)
本题解析:浓硫酸吸水,则A燃烧产生的水的质量是1.8g,物质的量是1.8g÷18g/mol=0.1mol。氢氧化钙吸收CO2生成碳酸钙,质量是20g,则碳酸钙的物质的量=20g÷100g/mol=0.2mol。根据碳原子守恒可知生成的CO2的物质的量是0.2mol。根据质量守恒定律可知,A分子中氧原子的质量=4.2g-0.1mol×2×1g/mol-0.2mol×12g/mol=1.6g,氧原子的物质的量是1.6g÷16g/mol=0.1mol,所以C、H、O三种原子的最简个数之比是0.2:0.2:0.1=2:2:1,因此A的最简式为C2H2O。
(2)A的相对分子质量为84,则分子中氧原子的个数是84÷42=2个,所以A的化学式为C4H4O2。
(3)8.4gA和足量银氨溶液反应,最终生成43.2g银,这说明A分子中含有醛基。A的物质的量是0.1mol,生成单质银的物质的量是43.2g÷108g/mol=0.4mol。由于1mol醛基只能生成2mol银,这说明A分子中含有2个醛基,因此A的结构简式为 。
。
本题难度:一般
5、填空题 为测定某有机化合物X的结构,进行如下实验:
(1)取一定量有机物X在氧气中完全燃烧,测得生成8.8g CO2和3.6g H2O,消耗标准状况下的氧气5.6L,则X中含有?种元素。
(2)用质谱仪测得A的相对分子质量为44,则X的分子式为?。
(3)根据价键理论,试写出X可能的结构简式(不考虑含有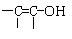 结构的物质)?。
结构的物质)?。
(4)X的核磁共振氢谱中出现两个不同位置的峰,则X与氢气反应的化学方程式是?。
参考答案:(1)3?(2)C2H4O?(3)CH3CHO?或  ?(每个1分)
?(每个1分)
(4)CH3CHO + H2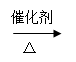 CH3CH2OH
CH3CH2OH
本题解析:(1)n(CO2)=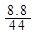 =0.2mol,n(H2O)=
=0.2mol,n(H2O)=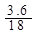 =0.2mol,n(O2)=
=0.2mol,n(O2)= ?="0." 25mol
?="0." 25mol
根据质量守恒定律,除碳、氢外,还有氧元素,则有机物中含n(O)=0.2mol×2+0.2mol-0.5mol=0.1mol,则有机物中N(C):N(H):N(O)=0.2mol:0.4mol:0.1mol=2:4:1,
(2)有机化合物的相对分子质量为44,则该物质的分子式是C2H4O;
本题难度:一般