|
高中化学知识点总结《有关氧化还原反应的计算》答题技巧(2020年最新版)(十)
2021-02-18 04:54:41
【 大 中 小】
|
1、选择题 设NA为阿伏加德罗常数的值。下列说法正确的是 ( )
A.标准状况下,2.24 L水中所含的电子数为NA
B.常温常压下,16 g O3所含的电子数为8NA
C.0.1 mol Na2O2晶体中所含的离子数为0.4NA
D.1 mol Fe在氧气中充分燃烧失去的电子数为3NA
|
参考答案:B
本题解析:A.标准状况下,水是液态,不能使用气体摩尔体积,错误;B.常温常压下,16 g O3含有的O原子的物质的量是1mol,所以所含的电子数为8NA,错误;C.0.1 mol Na2O2晶体中所含的离子数为0.3NA,错误;D. Fe在氧气中充分燃烧产物是Fe3O4,其中1/3s +2价,2/3是+3价,所以失去的电子数小于3NA,错误。
考点:考查阿伏加德罗常数的计算的知识。
本题难度:一般
2、选择题 下列化学用语表示正确的是
A.CO2分子的比例模型示意图: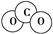
B.三氟化氮的电子式: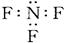
C.二氧化硅的分子式:SiO2
D.含有10个中子的氧原子: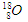
参考答案:D
本题解析:CO2分子的比例模型为 。三氟化氮中每个氟原子还有3对电 。三氟化氮中每个氟原子还有3对电
子对没有参与成键,正确的为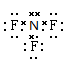 。在二氧化硅中不存在分子,SiO2代表化学式。所以正 。在二氧化硅中不存在分子,SiO2代表化学式。所以正
确的答案是D。
本题难度:简单
3、填空题 我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时会产生N2、CO2等。
(1)爆炸时的化学方程式为:?。(2分)
(2)在黑火药爆炸的反应中硫作氧化剂,在一些反应中硫也可以作还原剂,写出一个硫在反应中作还原剂的化学方程式:?。(2分)
(3)氮气在放电条件下与氧气反应的化学方程式:?。(2分)
(4)一氧化氮、二氧化氮都是氮氧化物。一氧化氮在常温下很容易与空气中的氧气化合,化学方程式为:??。(2分)二氧化氮能与水反应,化学方程式为:??。(2分)
参考答案:(1)S+3C+2KNO3 K2S+N2↑+3CO2↑(2分) (2)S+O2 K2S+N2↑+3CO2↑(2分) (2)S+O2 SO2(2分) SO2(2分)
(3)N2+O2 2NO(2分) (4)2NO+O2=2NO2(2分);3NO2+H2O=2HNO3+NO(2分) 2NO(2分) (4)2NO+O2=2NO2(2分);3NO2+H2O=2HNO3+NO(2分)
本题解析:(1)木炭、硫磺、硝石在点燃的条件下生成硫化钾、氮气和二氧化碳,反应的化学方程式为S+3C+2KNO3 K2S+N2↑+3CO2↑。 K2S+N2↑+3CO2↑。
(2)还原剂失去电子,化合价升高,例如硫在氧气中燃烧生成SO2,反应的化学方程式为S+O2 SO2。 SO2。
(3)氮气在放电的条件下生成NO,反应的化学方程式为N2+O2 2NO。 2NO。
(4)一氧化氮在常温下很容易与空气中的氧气化合生成NO2,反应的化学方程式为2NO+O2=2NO2;NO2溶于水生成NO和硝酸,反应的化学方程式为3NO2+H2O=2HNO3+NO。
本题难度:一般
4、填空题 写出下列反应的化学方程式:
(1)食品疏松剂中含有的碳酸氢钠在蒸煮时受热分解
(2)淀粉在人体消化道中转化为葡萄糖.
参考答案:(1)碳酸氢盐受热易分解为碳酸盐、水和二氧化碳,即2NaHCO3?△?.?Na2CO3+CO2↑+H2O,故答案为:2NaHCO3?△?.?Na2CO3+CO2↑+H2O;
(2)淀粉水解的主要产物是葡萄糖,即(C6H10O5)n+nH2O ?酸?.?nC6H12O6,故答案为:(C6H10O5)n+nH2O ?酸?.?nC6H12O6.
本题解析:
本题难度:一般
5、填空题 漂白粉的有效成分是①______,在使用漂白粉时为了增强漂白效果,可向溶液中滴加少量食醋(主要成分为CH3COOH),其原理用化学方程式表示为②______,如果不滴加食醋照样可以漂白,原理用化学方程式表示为③______.
参考答案:①根据漂白粉是混合物,主要成分是Ca(ClO)2和CaCl2,有效成分是Ca(ClO)2,
故答案为:Ca(ClO)2;
②根据强酸制弱酸的原理,CH3COOH酸性大于HClO,所以Ca(ClO)2+2CH3COOH=(CH3COO)2Ca+2HClO,
故答案为:Ca(ClO)2+2CH3COOH=(CH3COO) 2Ca+2HClO;
③漂白粉的有效成分为Ca(ClO)2,因Ca(ClO)2能与空气中的二氧化碳和水反应生成次氯酸:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO,
故答案为:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO.
本题解析:
本题难度:一般
|