1、选择题 工业上要冶炼金属钠,可使用的方法是(?)
A.电解法
B.加热分解法
C.还原剂加热法
D.铝热剂法
2、选择题 科学家致力于二氧化碳的组合转化技术研究,把过多的二氧化碳转化为有益于人类的物质,如将CO2和H2O以1∶4的比例混合,通入反应器,在适当的条件下反应,可获得一种重要的能源。请完成以下化学方程式:CO2+4H2 (?)+2H2O
(?)+2H2O
若将二氧化碳与氢气混合,在一定条件下以1∶3的比例发生反应,生成某种重要的化工原料和水,该化工原料可能是(?)
A.烷烃
B.烯烃
C.炔烃
D.芳香烃
3、填空题 碳酸锂广泛应用于陶瓷和医药等领域,以锂辉石(主要成分为LiAlSi2O6)为原材料制备Li2CO3的工艺流程如下:
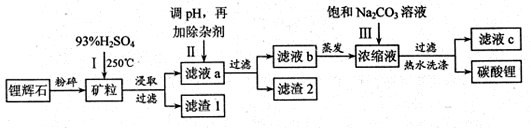
已知①2LiAlSi2O6+H2SO4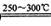 Li2SO4+Al2O3・4SiO2?H2O
Li2SO4+Al2O3・4SiO2?H2O
②Fe3+、Al3+、Fe2+和Mg2+以氢氧化物形式完全沉淀时,溶液的PH分别为3.2、4.7、9.0和11.1
③某些物质的溶解度(S)如下表

请回答下列问题:
(1)锂辉石用浓硫酸浸取之前要粉碎成细颗粒的目的是?。
(2)滤液a中含有Li+、SO42-,另含有Fe3+、Al3+、Fe2+、 Mg2+ ?、Ca2+?、Na+等杂质,步骤Ⅱ需在搅拌下加入石灰石以调节溶液的PH到6.0―6.5,此时沉淀的杂质离子有?;石灰石调节溶液PH的原理的离子方程式为?。
(3)步骤Ⅱ在滤液a中加入的除杂剂依次为适量的H2O2溶液,石灰乳和Na2CO3溶液,发生氧化还原反应的离子方程式为?。
(4)步骤Ⅲ中加入饱和Na2CO3溶液过滤后需要用热水洗涤的原因是?。
(5)从滤液c中可回收的主要物质是?。
4、选择题 下列关于海水资源的说法不正确的是(?)
A.海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等
B.从海水中可以提取铀和重水等核原料
C.海水中的溴、氟等元素均为微量元素,但仍有提取的价值
D.海水中金的储存量约为陆地的170倍,但它的富集程度却很低
5、填空题 (10分)空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:
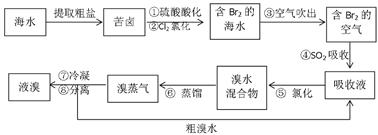
(1)溴在周期表中位于_________周期,_________族。
(2)步骤④的离子方程式:________________________________________?。
(3)步骤⑥的蒸馏过程中,溴出口温度为何要控制在80―90℃。温度过高或过低都不利于生产,请解释原因:___________________________________________?。
(4)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离。若在实验室分离上述混合物的分离仪器的名称是___________,分离时液溴从分离器的_________(填“上口”或“下口”)排出。
(5)为什么不直接用含溴的海水进行蒸馏得到液溴,而要经过“空气吹出、SO2吸收、氯化”:?。