1、填空题 (5分)下图中表示A~E五种物质的转化关系。
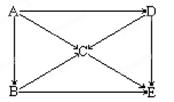
若将它们灼烧,火焰都呈黄色;A能跟水起剧烈反应,D常用作潜水艇里的氧气来源,E是生活中被称为纯碱的盐(物质间的反应均为一步反应)。试推断A~E各物质(写化学式):?
A??B??C??D??E?
参考答案:(5 分)A? Na?B? Na2O?
分)A? Na?B? Na2O? ??C? NaOH ?D? Na2O2??E? Na2CO3
??C? NaOH ?D? Na2O2??E? Na2CO3
本题解析:略
本题难度:一般
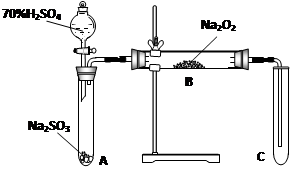
2、实验题 (12分)类比思想是化学学习常用的方法。已知Na2O2能与CO2反应,甲同学受到启发,提出一个相似的观点:Na2O2与SO2也能够反应。该同学用下图所示的装置进行实验,充分反应,B中固体由淡黄色变为白色(Na2O2完全反应),将带火星的木条插入试管C中,木条复燃。
 试回答下列问题:
试回答下列问题:
(1)请写出Na2O2与CO2反应的化学方程式:_________________?________________。
 (2)
(2) 乙同学认为此装置存在缺陷,请你帮其完成装置的改进并简述理由:
乙同学认为此装置存在缺陷,请你帮其完成装置的改进并简述理由:
 ①在A、B之间加一个干燥管,
①在A、B之间加一个干燥管, 理由_________________?________________。
理由_________________?________________。
 ②在B、C之间加一个装有?溶液的洗气瓶,
②在B、C之间加一个装有?溶液的洗气瓶, 理由_______________________。
理由_______________________。
(3) 任何的推论都要经过检验,请完成对白色固体成分的探究:
任何的推论都要经过检验,请完成对白色固体成分的探究: 限选实验试剂:稀盐酸、硝酸、NaOH稀溶液、蒸馏水、BaCl2溶液、澄清石灰水、品红溶液。
限选实验试剂:稀盐酸、硝酸、NaOH稀溶液、蒸馏水、BaCl2溶液、澄清石灰水、品红溶液。
 ①提出合理假设:
①提出合理假设:
 假设1:白色固体为Na2SO3;
假设1:白色固体为Na2SO3;
假设2:白色固体为Na2SO3与Na2SO4的混合物;
 假设3: ? 。
假设3: ? 。
 ②设计实验方案证明以上三种假设,完成下列填空。
②设计实验方案证明以上三种假设,完成下列填空。
步骤1:SO32-检验:取少量白色固体于试管,加入足量的?,塞上单孔胶塞,将生成的气体通入品红溶液。
步骤2:SO42-检验:在步骤1反应后的溶液中加入足量的?。
步骤3:结论: 若步骤1现象明显,而步骤2没明显现象,则假设1成立;若步骤1现象不明显,步骤2现象明显,则假设3成立;若上述两个实验现象均有,则假设2成立。
若步骤1现象明显,而步骤2没明显现象,则假设1成立;若步骤1现象不明显,步骤2现象明显,则假设3成立;若上述两个实验现象均有,则假设2成立。
参考答案:(12分)(1)2Na2O2 + 2CO2 ===?2Na2CO3 + O2?(2分)
(2)①产生的二氧化硫没有干燥,水蒸气会与Na2O2反应?(2分)
[②NaOH?(2分)除去SO2气体,防止污染空气(2分)
(3)①假设3:白色固体为Na2SO4(2分)②步骤1:稀盐酸;? (1分)
步骤2:氯化钡溶液;(1分)
本题解析:(1)Na2O2与CO2反应的化学方程式是2Na2O2 + 2CO2 ===?2Na2CO3 + O2。
(2)①由于生成的SO2中含有水蒸气,而水蒸气也能和过氧化钠反应生成氧气,所以需要在A、B之间加一个干燥管,用来干燥SO2。
②由于SO2是大气污染物,所以需要在B、C之间加一个装有氢氧化钠溶液的洗气瓶,除去SO2气体,防止污染空气。
(3)①根据假设1和假设2可知,假设3应该是白色固体为Na2SO4。
②亚硫酸钠能溶于盐酸中生成能使品红溶液褪色的SO2气体,所以加入的试剂应该是盐酸;SO42-的检验一般用氯化钡溶液,所以加入的试剂是氯化钡。2的制备、离子的检验等
点评:化学是一门以实验为基础的学科,所以有化学实验即科学探究之说法,这些实验主要以考察探究性实验和物质制备实验为主。这些探究性和制备性实验的试题,综合性强,理论和实践的联系紧密,有的还提供一些新的信息,这就要求学生必须认真、细致的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能得出正确的结论。
本题难度:一般
3、选择题 钠在干燥空气中形成的氧化物0.70g,溶于水后,可被100g质量分数为0.73%的盐酸恰好中和,钠的氧化物的成分是(?)
A.Na2O2和Na2O
B.Na2O
C.Na2O2
D.无法确定
参考答案:A
本题解析:由于不知道产物是 Na2O还是Na2O2,或者二者都有,因此设定一个化学式Na2OX,算出摩尔质量,与两种氧化物的对比即可判断。
n(盐酸)=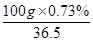 =0.02mol
=0.02mol
溶液恰好能被100g?质量分数为0.73%的盐酸溶液中和
则? Na2OX?~2NaOH~2HCl
0.01mol?0.02mol
则Na2OX平均摩尔质量M=0.70g÷0.01mol=70g/mol,介于Na2O(62g/mol)和Na2O2(78g/mOl)之间,因此,一定条件下钠与氧气反应的生成物是Na2O 和Na2O2,答案选A。
点评:该题是高考中的常见题型,属于中等难度的试题。试题在注重基础知识巩固与训练的同时,侧重对学生能力的培养和解题方法的指导与训练。解题若用极限法计算,计算比较繁琐,而用平均摩尔质量来求,则比较简单,注意方法规律的总结和积累。
本题难度:一般
4、选择题 向100mL2mol/L的NaOH溶液中通入一定量的CO2,结晶,得到9.3g白色固体,该白色固体的组成是
A.只含Na2CO3
B.只含NaHCO3
C.NaOH和Na2CO3的混合物
D.Na2CO3和NaHCO3的混合物
参考答案:C
本题解析:100mL2mol/L的NaOH溶液中通入一定量的CO2,产物的以下三种情况:
NaOH和Na2CO3的混合物,此时产物的质量范围是:8g~10.6g
②只含Na2CO3,此时产物的质量是:10.6g
③Na2CO3和NaHCO3的混合物,此时产物的质量范围是:10.6g~16.8g
④只含NaHCO3,此时产物的质量是: 16.8g
综上所述,选C。
本题难度:一般
5、选择题 将钠投入滴有石蕊的水中,下列有关的现象叙述错误的是
A.钠浮在水面
B.钠熔成闪亮的小球并在水面四处游动
C.有气体产生
D.水溶液变红色
参考答案:D
本题解析:滴入酚酞的溶液显红色
本题难度:简单