1、填空题 海水占地球总储水量的97.2%.若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源.
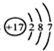
(1)海水中含有大量的氯化钠.请写出氯原子的原子结构示意图______;
(2)目前国际上实用的“海水淡化”主要技术之一是蒸馏法.蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水,由此可判断蒸馏法是______(填物理变化、化学变化);
(3)工业上利用电解饱和食盐水可制得重要化工产品,又称为“氯碱工业”.电解饱和食盐水的化学方程式为______;
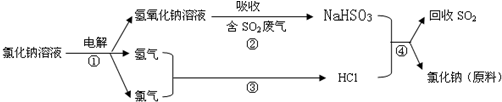
(4)近年来有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废气并回收二氧化硫的方法,该方法的流程如下:试写出④的化学反应方程式______.
参考答案:(1)根据氯原子的原子序数17,则氯原子的原子结构示意图为:
,
(2)由于蒸馏法只是水的状态由液态到气态再到液态的过程,所以属于物理变化;
(3)根据电解原理,可得2NaCl+2H2O?电解?.?2NaOH+H2↑+Cl2↑;
(4)因弱酸的酸式盐能与强酸反应:NaHSO3+HCl=NaCl+SO2↑+H2O;
故答案为:(1)

?
(2)物理变化?
(3)2NaCl+2H2O?电解?.?2NaOH+H2↑+Cl2↑
(4)NaHSO3+HCl=NaCl+SO2↑+H2O
本题解析:
本题难度:一般
2、简答题 有关1735Cl-粒子,回答下列问题:?
(1)所含质子数______;中子数______,电子数______;质量数______.?
(2)该粒子的结构示意图______.
(3)1735Cl-与1735Cl、1737Cl之间的关系是______.?
(4)1735Cl-与1735Cl的半径大小的关系是______.?
参考答案:(1)1735Cl-的质子数为17,质量数为35,中子数=35-17=18,核外电子=质子数+1=17+1=18,
故答案为:17;18;18;35;
(2)该粒子是氯离子,所以离子结构示意图为:
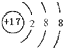
,故答案为:
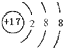
.
(3)因决定元素种类的是质子数,而1735Cl-与1735Cl、1737Cl的质子数相等,所以它们是同种元素的不同粒子,
故答案为:氯元素的不同粒子.
(4)因同种元素的原子和离子的半径大小取决于核外电子数,核外电子数越多,半径越大,
所以半径:1735Cl->1735
Cl,故答案为:1735Cl->1735Cl.
本题解析:
本题难度:一般
3、选择题 下列化学用语使用正确的是( ? )
A.HCN分子的结构式:H-C≡N
B.水分子的球棍模型:
C.F-离子的结构示意图:
D.二氧化碳的电子式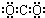
参考答案:A
本题解析:
本题难度:一般
4、选择题 下列化学用语的书写正确的是
[? ]
A.乙酸的分子式:C2H4O2
B.乙醇的结构简式:C2H6O
C.F原子结构示意图: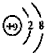
D.四氯化碳的电子式:
参考答案:A
本题解析:
本题难度:简单
5、选择题 下列有关化学用语正确的是( )
A.CO2的结构式:O-C-O
B.Cl-的结构示意图: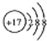
C.NH3分子比例模型:
D.质量数为37的氯原子:
参考答案:B
本题解析:
本题难度:一般