1、选择题 一定温度下,将CI2缓缓通入水中至饱和,然后向所得饱和氯水中滴加0.1mol/L的NaOH溶液,溶液PH变化的曲线如图所示。则下列叙述中正确的是
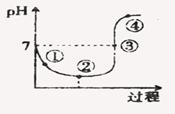
A.点①所示溶液中c(H+) =c(C l-)+c(HClO)+c(OH-)
B.点②所示溶液中:c(H+)>c(Cl-)>c(ClO-)>c(HClO)
C.点③所示溶液中:c(Na+)=2c(ClO-)+c(HClO)
D.点④所示溶液中:c(Na+)>c(ClO-)>c(Cl-)>c(HClO)
参考答案:C
本题解析:氯水中存在平衡Cl2+H2O Cl-+H++HClO。根据电荷守恒可知,c(H+) +c(Na+)=c(C l-)+ c(ClO-)+c(OH-),①②显酸性,A、B都不正确。③显中性,C正确,④显碱性,D不正确,答案选C。
Cl-+H++HClO。根据电荷守恒可知,c(H+) +c(Na+)=c(C l-)+ c(ClO-)+c(OH-),①②显酸性,A、B都不正确。③显中性,C正确,④显碱性,D不正确,答案选C。
本题难度:简单
2、选择题 下列叙述正确的是
A.氨水是强碱
B.含金属元素的离子不一定是阳离子
C.凡能电离出H+的化合物均属酸
D.盐类物质一定含有金属阳离子
参考答案:B
本题解析:氨水是弱碱,A不正确;B正确,例如MnO4-等;C不正确,例如硫酸氢钠,应该是电离出的阳离子全部是氢离子的化合物是酸;D不正确,例如铵盐等,答案选B。
点评:该题是基础性试题的考查,试题难易适中,侧重对学生基础性知识的巩固和检验,难度不大。该题的关键是熟练记住常见的化学基本概念,然后灵活运用即可。另外还需要学会通过举例逐一排除得出举例的解题方法。
本题难度:简单
3、选择题 在常温下,pH = 9的NaOH溶液和CH3COONa两种溶液中,假设由水电离产生的OH─离子浓度分别为a和b,则a与b的关系为
A.a>b
B.a=10-4b
C.b =10-4 a
D.a =b
参考答案:B
本题解析:氢氧化钠是强碱,抑制水的电离,则由水电离产生的OH─离子浓度为10-9mol/L;醋酸钠是强碱弱酸盐,水解促进水的电离,则由水电离产生的OH─离子浓度为10-5mol/L,所以a与b的关系是a=10-4b,答案选B。
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,侧重对学生能力的培养和解题方法的指导和训练,该题的关键是明确外界条件是如何影响水的电离平衡的,有利于培养学生的逻辑推理能力,提高学生的答题能力。
本题难度:一般
4、选择题 100 mL pH=2的两种一元酸x和y,稀释过程中pH与溶液体积的关系如图所示。下列说法正确的是
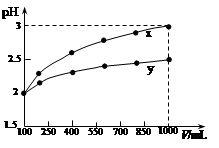
A.稀释前x、y的物质的量浓度相等
B.x为强酸,y为弱酸
C.随着稀释的进行,y的电离程度减小
D.等体积的x、y分别分别与足量的锌反应,x放出的氢气多
参考答案:B
本题解析:根据图像可知,稀释10倍,X的pH从2变为3,所以X是强酸,但Y的pH从2变为2.5,这说明在稀释过程中,有氢离子电离出来,所以Y是弱电解质,因此B正确。A不正确,稀释前Y的浓度大,C不正确,稀释促进电离。D不正确,应该是是Y发出的氢气多,答案选B。
本题难度:简单
5、选择题 下列表示的离子方程式正确的是(?)
A.NH NO
NO 溶液与氢氧化钠共热:
溶液与氢氧化钠共热:
H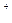 +OH-
+OH- H
H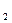 O
O
B.NH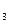 ・H
・H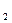 O滴入AlCl3溶液产生沉淀:
O滴入AlCl3溶液产生沉淀:
3OH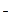 +Al
+Al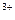
 Al(OH)
Al(OH)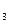 ↓
↓
C.NaOH溶液与NaHCO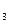 溶液混合:
溶液混合:
OH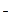 +H
+H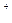
 H
H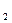 O
O
D.Al(OH)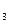 固体溶于稀硫酸中:
固体溶于稀硫酸中:
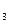 +3H
+3H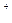
 Al
Al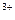 +3H
+3H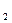 O
O