1、计算题 如图所示支管中,左管中放入KMnO4固体,右管中放入一小块钠,再向两管均加入适量8mol・L-1的盐酸,半分钟后,盖以橡胶塞并将此支管固定在铁架台上。用一照相机对准此支管,按快门,闪光灯闪亮。请回答:
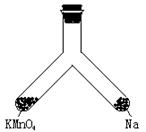
(1)“照像”之前,左管中反应的离子方程式__________________________。
(2)“照像”时,灯光闪亮,支管随之出现的现象为______________________,
化学方程式为_______________________________________。
参考答案:(1)2MnO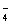 +16H++10Cl-==2Mn2++8H2O+5Cl2↑
+16H++10Cl-==2Mn2++8H2O+5Cl2↑
(2)支管内气体发生爆炸,胶塞被冲出支管口?H2+Cl2 2HCl
2HCl
本题解析:左边浓盐酸与高锰酸钾反应生成氯气,高锰酸钾中+7价锰被还原为Mn2+。右边浓盐酸金属钠反应生成氢气,与在光照条件下,氯气和氢气发生反应生成氯化氢并发生爆炸。
本题难度:简单
2、选择题 已知某植物营养液的配方含0.3molKCl、0.2molK2SO4、0.1molZnSO4和1LH2O。若以KCl、K2SO4、ZnCl2和1LH2O为原料配得相同组成的营养液,需 KCl、K2SO4、ZnCl2物质的量分别是
A.0.3mol、0.2mol、0.1mol
B.0.1mol、0.2mol、0.3mol
C.0.1mol、0.3mol、0.1mol
D.0.1mol、0.2mol、0.1mol
参考答案:C
本题解析:0.1molZnSO4中有0.1molZn2+,0.1molSO42―;0.3molKCl中有0.3molK+,0.3molCl―;0.2molK2SO4中有0.4molK+,0.2molSO42―;根据质量守恒定律可得:需 KCl、K2SO4、ZnCl2物质的量分别是0.1mol、0.3mol、0.1mol;
本题难度:一般
3、选择题 在150°C时,(NH4)2CO3完全分解产生的混合气体,其密度是相同条件下氢气密度的
[? ]
A、96倍
B、48倍
C、32倍
D、12倍
参考答案:D
本题解析:
本题难度:一般
4、选择题 检测据报道,科学家已成功合成了少量的O4,有关O4的说法正确的是
A.O4的摩尔质量是64 g
B.相同质 量的O4与O3所含原子个数之比为1∶1
量的O4与O3所含原子个数之比为1∶1
C.O4与O2互为同位素
D.O4与O3、O2都是氧元素的同分异构体
参考答案:B
本题解析:略
本题难度:一般
5、选择题 设NA表示阿伏加德罗常数的值,下列叙述正确的是( )。
A.10 g氖气中所含的原子数为NA
B.9 g重水含有的电子数为5 NA
C.标准状况下,将22.4 L氯化氢气体溶于足量水中,溶液中含有的氯化氢分子数为NA
D.常温常压下,22 g CO2中含有NA个C=O键
参考答案:D
本题解析:氖气为单原子分子,10 g氖气的物质的量为0.5 mol,所含原子数0.5NA,A错;9 g重水含有的电子数为 ×10NA=4.5NA,B错。盐酸中不存在氯化氢分子,C错;CO2的结构式为O=C=O,22 g CO2中含有1 mol(即NA个)C=O键,D正确。
×10NA=4.5NA,B错。盐酸中不存在氯化氢分子,C错;CO2的结构式为O=C=O,22 g CO2中含有1 mol(即NA个)C=O键,D正确。
本题难度:简单