1、选择题 在一真空密闭容器中通入5 mol H2和8 mol N2,在某一时刻二者化合得到2 mol NH3(假设温度保持不变),此时容器内的压强是反应前压强的(? )
A.0.25倍
B.1.75倍
C.0.85倍
D.4倍
参考答案:C
本题解析:反应前,气体的物质的量为(5+8) mol="13" mol,根据
N2+3H2 2NH3? Δn
2NH3? Δn
1? 3? 2? 2
当生成2 mol NH3,气体减少2 mol,故反应后气体物质的量为(13-2) mol="11" mol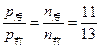 =0.85。
=0.85。
本题难度:简单
2、选择题 在标准状况下,将a L NH3完全溶于水得到V mL氨水,溶液的密度为ρ g・cm-3,溶质的质量分数为w,溶质的物质的量浓度为c mol・L-1。下列叙述中正确的是( )
①w=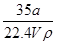 ×100%
×100%
②c=
③若上述溶液中再加入V mL水后,所得溶液的质量分数大于0.5w
④若上述溶液中再加入0.5V mL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为c(NH4+)>c(Cl-)>c(OH-)>c(H+)
A.①④
B.②③
C.①③
D.②④
参考答案:D
本题解析:①w=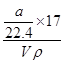 ×100%=
×100%=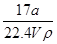 ×100%;②c=
×100%;②c=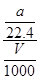 =
= ;③因为V mL水的质量大于V mL氨水的质量,所以溶液的质量分数小于0.5w;④所得溶液为NH4Cl和NH3・H2O等物质的量的混合液,所以c(NH4+)>c(Cl-)>c(OH-)>c(H+)。
;③因为V mL水的质量大于V mL氨水的质量,所以溶液的质量分数小于0.5w;④所得溶液为NH4Cl和NH3・H2O等物质的量的混合液,所以c(NH4+)>c(Cl-)>c(OH-)>c(H+)。
本题难度:一般
3、选择题 (8分)(1)2 mol O3和3 mol O2的质量之比________,体积之比________.
(2)若12.4 g Na2X中含有0.4 mol钠离子,Na2X的摩尔质量是________ X的相对原子质量是________.
参考答案:(1)1∶1? 2∶3
(2)62 g・mol-1? 16
本题解析:(1)O3和O2都是氧元素单质,质量比等于氧原子个数比,1∶1;根据阿伏伽德罗定律,气体体积比等于气体物质的量之比,2∶3。
(2) 12.4 g Na2X中含有0.4 mol钠离子,则Na2X为0.2mol,M(Na2X)=" 12.4" g/0.2mol="62" g・mol-1;X的相对原子质量=62-46=16。
本题难度:一般
4、填空题 (3分)将足量BaCO3分别加入:① 30mL 水 ②10mL 0.2mol/LNa2CO3溶液 ③50mL 0.01mol/L 氯化钡溶液 ④100mL 0.01mol/L盐酸中溶解至溶液饱和。请确定各溶液中Ba2+的浓度由大到小的顺序为: _____
参考答案:
本题解析:
① 30mL 水,BaCO3正常电离② 0.2mol・L-1Na2CO3溶液,BaCO3电离程度变小,③50mL 0.01mol/L 氯化钡溶液,BaCO3电离程度变小,但比Ba2+ 浓度大,比0.01mol/L略大;④100mL 0.01mol/L盐酸中溶解至溶液饱和,Ba2+ 约是0.005mol/L。Ba2+ 的顺序为③④①②。
本题难度:一般
5、选择题 某KCl、MgCl2、Mg(NO3)2形成的混合液中,c(K+)=0.1mol/L,
c(Mg2+)=0.25mol/L,c(Cl-)=0.2mol/L,则c(NO3-)为? (?)
A.0.15mol/L
B.0.10mol/L
C.0.25mol/L
D.0.40mol/L
参考答案:D
本题解析:略
本题难度:简单