1、选择题 在一定温度下,反应H2(g)+X2(g) 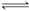 HX(g)的平衡常数为10。若将1.0 mol的HX(g)通入体积为1.0 L的密闭容器中,在该温度时HX(g)的最大分解率接近于( )
HX(g)的平衡常数为10。若将1.0 mol的HX(g)通入体积为1.0 L的密闭容器中,在该温度时HX(g)的最大分解率接近于( )
A.5%
B.17%
C.25%
D.33%
参考答案:B
本题解析:反应H2(g)+X2(g) 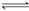 HX(g)中,HX(g)的最大分解率即达到平衡状态;
HX(g)中,HX(g)的最大分解率即达到平衡状态;
根据反应:HX(g) 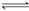 H2(g)+X2(g)
H2(g)+X2(g)
起始浓度? 1? 0? 0
变化浓度? 2x? x? x
平衡浓度 1-2x? x? x
由于反应H2(g)+X2(g)  HX(g)的平衡常数为10,则HX(g)
HX(g)的平衡常数为10,则HX(g)  H2(g)+X2(g)的平衡常数为
H2(g)+X2(g)的平衡常数为 ;所以
;所以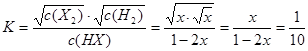 ;解得
;解得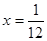 ;在该温度时HX(g)的最大分解率=
;在该温度时HX(g)的最大分解率=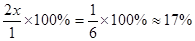
本题难度:一般
2、选择题 在一定温度下,向a L密闭容器中加入1mol X气体和 2mol Y气体,发生如下反应:X(g)+2Y(g)  2Z(g),此反应达到平衡的标志是? ( )
2Z(g),此反应达到平衡的标志是? ( )
A.容器内压强不随时间变化
B.v正(X)=v逆(Z)
C.容器内X、Y、Z的浓度之比为1:2:2
D.单位时间消耗0.1mol X同时生成0.2mol Z
参考答案:A
本题解析:在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。该反应是体积减小的可逆反应,则压强也是减小的,所以当压强不再发生变化时,可以说明,A正确;B中反应速率的方向相反,但不能满足速率之比是相应的化学计量数之比,不正确。平衡时各种物质的浓度不再发生变化,但各种的浓度之间不一定满足某种关系,C不能说明。D中反应速率的方向相同,速率之比是相应的化学计量数之比,因此D中的关系始终是成立,不正确,因此答案选A。
点评:该题是中等难度的试题,也是高考中的常见题型和考点。试题基础性强,难易适中,侧重对学生能力的培养和解题方法的指导与训练,有助于培养学生的逻辑推理能力和发散思维能力。该题的关键是明确平衡状态的特点,然后结合具体的可逆反应灵活运用即可。
本题难度:一般
3、选择题 如图所示,一定条件下将1mol A2气体和3molB2气体充入一容积可变的密闭容器中,可滑动的活塞的位置如图1所示。在恒温恒压下发生如下反应:A2+3B2? ?2AB3。当反应达到平衡时,活塞位置如图2所示,则平衡时A的转化率是
?2AB3。当反应达到平衡时,活塞位置如图2所示,则平衡时A的转化率是
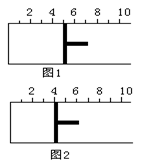
A.20%
B.40%
C.60%
D.无法确定
参考答案:B
本题解析:由题意知,反应前后气体的体积从5降至4,或者说反应前后物质的量比为:5:4
A2?+?3B2? ?2AB3
?2AB3
1mol ?3mol
a? 3a ?2a
1―a?3―3a? 2a
即:4:(4―2a) = 5:4?推出:a="0.4" mol
本题难度:一般
4、选择题 在一密闭容器中反应mA(g) nB(g)+nC(g)达到平衡。保持温度不变,将容器容积压缩到原来的一半,当达到新的平衡时,B和C的浓度均是原来的1.8倍。则
nB(g)+nC(g)达到平衡。保持温度不变,将容器容积压缩到原来的一半,当达到新的平衡时,B和C的浓度均是原来的1.8倍。则
A.平衡向逆反应方向移动
B.物质A的转化率增加
C.物质C的质量分数增加
D.m >2n
参考答案:A
本题解析:略
本题难度:一般
5、计算题 将1体积N2和4体积H2放入密闭容器中,测得压强为3.03×105Pa,达平衡后测得含NH3为12%,试求:
(1)平衡时N2和H2占平衡混合气体的体积百分比;
(2)到达平衡时的压强。
参考答案:(1)N2的百分含量:16.4%;H2的百分含量:71.6%
(2)平衡混合气的压强为2.70×105Pa
本题解析:
本题难度:一般