1、选择题 将有机物完全燃烧,生成CO2和H2O。将12 g 该有机物的完全燃烧产物通过浓H2SO4,浓H2SO4增重14.4 g,再通过碱石灰,碱石灰增重26.4 g。则该有机物的分子式为( )
A.C4H10
B.C2H6O
C.C3H8O
D.C2H4O2
参考答案:C
本题解析:浓H2SO4增重14.4 g,则水的质量是14.4g,物质的量是0.8mol。再通过碱石灰,碱石灰增重26.4 g,则CO2的质量是26.4g,物质的量是0.6mol,及有机物中碳氢原子的个数之比是3:8,则根据选项中有机物的分子式可知,答案选C。
点评:该题是中等难度的试题,试题基础性强,侧重能力的培养。试题主要是考查学生通过计算得出化学式的计算能力,有利于培养学生的逻辑思维能力和应试能力。
本题难度:一般
2、选择题 现有乙酸、环己烷、辛烯组成的混合物,其中氧的质量分数为a,则碳的质量分数是(?)
A.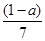
B.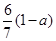
C.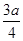
D.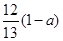
参考答案:B
本题解析:乙酸分子式为C2H4O2,环己烷分子式为C6H12,辛烯分子式为C8H16,他们形成的混合物中C、H原子个数比都为1:2,所以当氧的质量分数为a时,碳的质量分数为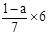 ,所以答案选B。
,所以答案选B。
点评:本题注意寻找元素个数的关系,找到对应关系就可以进行计算。
本题难度:一般
3、填空题 ( 15 分)
二甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能。四川是利用天然气生产二甲醚的重要基地之一。
请填写下列空白:
(1)与二甲醚相对分子质量相等且元素种类相同的有机物的结构简式是:
________________________________________________。
(2)二甲醚可由合成气(CO+H2)在一定条件下制得。用合成气制二甲醚时,还产生了一种可参与大气循环的无机化合物,该反应的化学方程式可能是:
________________________________________________。
(3)以二甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成然料电池。该电池中负极上的电极反应式是:______________________________________________________。?
(4)制备二甲醚的合成气可由甲烷与水燕气或二氧化碳经高温催化反应制得。合成气除制二甲醚外,还可用于冶炼金属,用它冶炼铁的生产过程可示意如下:
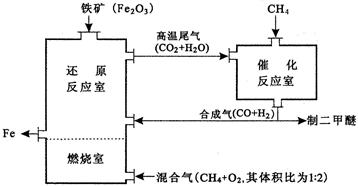
①在催化反应室中进行的反应均为可逆反应.增大体系的压强对甲烷转化率的影响是___________________________(填“增大”、“减小”或“不变”)。
②在上述炼铁过程的某时间段内,若有x m3(标准状况)的甲烷进入燃烧室中充分燃烧,还原反应室有5 y kg(y/11.2×103mol)铁生成,假设燃烧室与还原反应室产生的高温尾气全部进人催化反应室,则这些高温尾气在理论上可产生合成气_______________m3(标准状况)。
参考答案:
(1)CH3CH2OH、HCOOH
(2)3CO+3H2=CH3OCH3?或2CO+4H2=CH3OCH3+H2O
(3)CH3OCH3+16OH―-12e-=2CO32-+11H2O
(4)①减小
②12(x + y)
本题解析:略
本题难度:一般
4、选择题 下列关于有机化合物的结构、性质的叙述正确的是
A.苯、油脂均能使酸性KMnO4溶液褪色
B.甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应
C.蔗糖、麦芽糖的分子式均为C12H22O11,二者互为同分异构体
D.乙醇、乙酸均能与NaOH反应,因为分子中均含有官能团“―OH”
参考答案:C
本题解析:A、苯不能使酸性KMnO4溶液褪色,油脂中含有碳碳双键,能使酸性KMnO4溶液褪色,错误;B、甲烷和Cl2的反应属于取代反应,乙烯和Br2的反应属于加成反应,不是同一类型的反应,错误;C、蔗糖、麦芽糖的分子式均为C12H22O11,二者互为同分异构体,正确;D、乙酸能与NaOH反应,而乙醇与NaOH不反应,错误。
本题难度:一般
5、选择题 第一次用无机物制备有机物尿素,开辟人工合成有机物先河的科学家是(?)
A.德国的维勒
B.英国的道尔顿
C.德国的李比希
D.俄罗斯的门捷列夫
参考答案:A
本题解析:考查化学史。英国的道尔顿提出了原子学说,德国的李比希为现代元素定量分析奠定了基础。俄罗斯的门捷列夫绘制出第一张元素周期表。答案是A。
本题难度:简单