|
|
|
高考化学知识点总结《化学反应与能量》答题技巧(2020年最新版)(三)
2021-02-18 05:49:12
【 大 中 小】
|
1、选择题 已知N4分子的结构和P4(白磷)分子的结构相似(正四面体),断裂1mol N-N键吸收167kJ热量,生成
1mol N≡N键放出942kJ热量。下列说法正确的是
[? ]
A.N4与N2互为同素异形体
B.N4转变为N2将吸收热量
C.N4与P4互为同分异构体
D.制备N4的热化学方程式可表示为:2N2(g)=N4(g)△H=+1216kJ・mol-1
2、选择题 1g H2燃烧生成液态水放出142.9 kJ的热量,下列热化学方程式书写正确的是( )
A.2H2(g)+ O 2(g) = 2H2O (1), ΔH = ―142.9 kJ・mol-1
B.2H2(g)+ O 2(g) = 2H2O (1), ΔH = ―571.6 kJ・mol-1
C.2H2+O2 = 2H2O, ΔH = ―571.6 kJ・mol-1
D.H2(g)+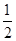 O 2(g) = H2O (1), ΔH = +285.8 kJ・mol-1 O 2(g) = H2O (1), ΔH = +285.8 kJ・mol-1
|
3、选择题 下列热化学方程式书写正确的是( )
A.C(s)+O2(g)=CO2(g)ΔH=+393.5 kJ/mol
B.2SO+O2=2SO3ΔH=-196.6 kJ/mol
C.H2(g)+1/2O2(g)=H2O(l)ΔH=-285.8 kJ/mol
D.2H2(g)+O2(g)=2H2O(l)ΔH=-571.6 kJ
|
4、选择题 某反应的△H=-80kJ・mol-1,叙述正确的是( )
A.正反应活化能等于80kJ・mol-1
B.逆反应活化能一定大于80kJ・mol-1
C.逆反应活化能不大于80kJ・mol-1
D.正反应活化能比逆反应活化能小80kJ・mol-1
5、填空题 (8分)水煤气不仅是合成氨的原料气也是合成烃及其化工产品的原料。
(1)在水煤气燃料电池中,通CO、H2的极为电池的 极(选填“正”、“负”)。
(2)水煤气变换反应:CO(g) + H2O(g)  CO2(g) + H2(g) △H<0,下列措施能提高反应速率的有 (不定项选择)。
CO2(g) + H2(g) △H<0,下列措施能提高反应速率的有 (不定项选择)。
a.升高温度 b.加入催化剂 c.增大压强 d.降低浓度
(3)H2和N2在催化剂、高温高压条件下合成氨的化学方程式为 。
(4)将标准状况下582.4L合成气[已知:n(CO)∶n(H2)= 4∶9]通入合成塔,一定条件下可发生2CO(g)+ 4H2(g) → CH2=CH2(g)+2H2O(g);CO(g)+3H2→CH4(g)+H2O(g),充分反应后,经测定产品中只有甲烷、乙烯和水蒸气(假定CO和H2均无剩余),逸出的气体中乙烯的物质的量为 。
 CO2(g) + H2(g) △H<0,下列措施能提高反应速率的有 (不定项选择)。
CO2(g) + H2(g) △H<0,下列措施能提高反应速率的有 (不定项选择)。