1、选择题 李敏同学欲配制250?mL?1.0?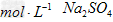 溶液,正确的方法是
溶液,正确的方法是
[? ]
①将35.5?g?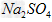 固体溶于250?mL水中?
固体溶于250?mL水中?
②将80.5?g?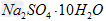 固体溶于少量水中.再用水稀释至250?mL?
固体溶于少量水中.再用水稀释至250?mL?
③将50?mL?5.0?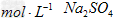 溶液用水稀释至250?mL?
溶液用水稀释至250?mL?
A.①②
B.②③
C.①③
D.①②③?
参考答案:B
本题解析:
本题难度:简单
2、选择题 配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
A.所用NaOH已吸潮
B.定容前溶液未冷却
C.称量时砝码位置放错
D.向容量瓶加水时眼睛一直仰视液面
参考答案:B
本题解析:
本题难度:一般
3、选择题 下列是在配制一定物质的量浓度的溶液中的操作(假设其他操作都正确),不会影响溶液的浓度的是
[?]
A.溶解溶质的烧杯,用蒸馏水洗涤后未烘干
B.向容量瓶转移溶液时有少许溶液溅至瓶外
C.未将洗涤烧杯的液体注入容量瓶即进行定容
D.定容时,眼睛的视线高于容量瓶的刻度线
参考答案:A
本题解析:
本题难度:简单
4、实验题 用18 mol/L的硫酸溶液配制500 mL1 mol/L的硫酸溶液,有下列操作步骤:
(1)将溶解后的硫酸溶液立即沿玻璃棒转入容量瓶中;
(2)将量得的浓硫酸倒入烧杯中,加水溶解,然后用蒸馏水洗涤量筒2~3次,倒入烧杯中;
(3)盖上瓶塞,轻轻摇匀即配制完毕;
(4)洗涤烧杯和玻璃棒2~3次,将洗涤液全部转入容量瓶中,加水至离刻度1~2 cm处,改用胶头滴管加水至刻度线;
(5)用量筒量取27. 78 mL的浓硫酸。
先将以上步骤按实际操作的先后顺序排列,_________指出操作中所有的错误和不妥之处____________。
参考答案:(5)(2)(1)(4)(3);
操作中的错误可按操作顺序的先后逐步检查:
量筒是粗量器具,只能量准到小数点后一位,量取27. 78 mL是不可能的;
溶解浓硫酸一定要将硫酸沿烧杯壁慢慢加入水中且边加边用玻璃棒搅拌,将水加入浓硫酸中是错误的;
量筒不用洗涤,洗涤量筒是错误的;
浓硫酸的溶解要放出大量热,不能立即转入容量瓶中,一定要冷却到室温;
洗涤2~3次烧杯和玻璃棒的洗涤液转入容量瓶后,要轻轻摇匀容量瓶一次,再注入蒸馏水定容反复摇匀。
本题解析:
本题难度:一般
5、简答题 某学生欲用已知物质的量浓度的HCl测定未知浓度的NaOH溶液,将HCl置于滴定管,氢氧化钠溶液置于锥形瓶,选择酚酞作指示剂.请填写下列空白:
(1)用标准的盐酸滴定未知浓度的NaOH溶液,滴定到终点时锥形瓶中颜色变化为______.
(2)下列操作中可能无法会怎样影响所测NaOH溶液浓度(填偏大、偏小或不影响)
A.酸式滴定管未用标准浓度的HCl润洗就直接注入标准盐酸______
B.读数时,开始平视,结束时俯视液面______
(3)某学生根据3次实验记录有关数据如下:
| 滴定次数 | 待测NaOH溶液体积(mL) | 0.1000mol/L?HCl溶液的体积(mL)
滴定前刻度
滴定后刻度
第一次
25.00
0.00
26.11
第二次
25.00
1.56
30.30
第三次
25.00
0.22
26.31
|
请选择合理的数据计算NaOH溶液的物质的量浓度:c(NaOH)=______.
参考答案:(1)酚酞遇碱变红,观察锥形瓶中溶液的颜色由浅红色变成无色,且半分钟内不恢复,达到滴定终点,
故答案为:溶液的颜色由浅红色变成无色,且半分钟内不恢复;
(2)利用c(碱)=c(酸)V(酸)V(碱)可知,
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸,盐酸被稀释,消耗酸的体积增大,则c(碱)偏大;
B.读取盐酸体积时,开始平视读数,读数正确,滴定结束时俯视读数,读数偏小,则差偏小,即消耗酸的体积偏小,所以c(碱)偏小,
故答案为:偏大;偏小;
(3)碱的体积相同,第二次消耗酸的体积更大,应舍去,利用第一次、第三次计算消耗的盐酸溶液的体积平均值=26.11+(26.31-0.22)2mL=26.10mL,故c(NaOH)=26.10mL×0.1mol/L25.00mL=0.1044mol/L,
故答案为:0.1044mol/L.
本题解析:
本题难度:一般