1、选择题 下表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是( )。
元素代号
| L
| M
| Q
| R
| T
|
原子半径/nm
| 0.160
| 0.143
| 0.089
| 0.102
| 0.074
|
主要化合价
| +2
| +3
| +2
| +6、-2
| -2
|
?
A.L2+与R2-的核外电子数相等
B.M与T形成的化合物既能与酸反应又能与强碱反应
C.氢化物的稳定性为H2T<H2R
D.单质与浓度相等的稀盐酸反应的速率为Q>L
参考答案:B
本题解析:根据R和T的化合价及原子半径可以推测:R是硫元素,T是氧元素,再根据Q、T、L的半径关系可以推测出Q是铍元素,L是镁元素,再根据L、M的半径关系和化合价推测M是铝元素。M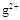 和
和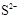 的核外电子数不相等,A错;Al2O3既能与酸反应又能与强碱反应,B正确;氢化物的稳定性H2S<H2O,C错;单质与浓度相同的盐酸反应的速率Be<Mg,所以D错误。
的核外电子数不相等,A错;Al2O3既能与酸反应又能与强碱反应,B正确;氢化物的稳定性H2S<H2O,C错;单质与浓度相同的盐酸反应的速率Be<Mg,所以D错误。
本题难度:一般
2、填空题 (1)A元素的负一价离子和B元素的正一价离子的电子层结构都与氩相同,A的离子结构示意图为?,B元素名称为?;
(2)C元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,C的元素基态原子的外围电子排布式为?.
(3)D元素的原子序数为33,该元素原子的核外电子共有?种不同的运动状态,此元素原子的核外电子排布式是?
(4)N≡N的键能为942kJ・mol-1,N―N单键的键能为247kJ・mol-1,通过计算说明N2中的?键更稳定(填“σ”或“π”)。
(5)下列4种物质熔、沸点由高到低排列为?(填序号).
①金刚石?②晶体锗?③晶体硅?④金刚砂
参考答案:(每空2分)(1)  ,钾;(2)3d104s1?(3)? 33 ;【Ar】3d104s24p3
,钾;(2)3d104s1?(3)? 33 ;【Ar】3d104s24p3
(4)π? (5)?①>④>③>②
本题解析:(1)A元素的负一价离子和B元素的正一价离子的电子层结构都与氩相同,则A和B分别是氯元素和钾元素,则A的离子结构示意图为 。
。
(2)C元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,所以C应该是铜元素,则根据构造原理可知,C的元素基态原子的外围电子排布式为3d104s1。
(3)D元素的原子序数为33,该元素原子的核外电子共有33种不同的运动状态。则根据构造原理可知,此元素原子的核外电子排布式是【Ar】3d104s24p3。
(4)氮气分子中的三键是由1个σ键和2个π键构成的,则π键键能是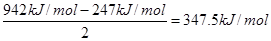 >247kJ/mol,所以π键比σ键稳定。
>247kJ/mol,所以π键比σ键稳定。
(5)四种物质形成的晶体都是原子晶体,原子晶体中原子半径越小,共价键越强,晶体的熔沸点越高。由于原子半径是C<Si<Ge,所以4种物质熔、沸点由高到低排列为①>④>③>②。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,贴近高考,试题在注重对基础知识巩固和训练的同时,更侧重对学生能力的培养和解题方法的指导与训练,有助于培养学生逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力。
本题难度:一般
3、选择题 根据元素周期表和元素周期律,下列推断中正确的是
A.溴化氢比氯化氢稳定,HClO4酸性强于HBrO4
B.在周期表中金属和非金属元素的分界线附近可以寻找制取新农药的元素
C.铷的硫酸盐易溶解于水,其氢氧化物一定是弱碱
D.砹是一种有色固体,它的气态氢化物很不稳定,
参考答案:D
本题解析:略
本题难度:简单
4、选择题 某元素原子的最外层电子数为次层电子数的3倍,则该元素原子核内质子数为(?)
A.3
B.7
C.8
D.10
参考答案:C
本题解析:可根据核外电子排布规律和题干中所给的信息画出该元素原子的结构示意图,然后对照选项,选出正确答案。
根据原子核外电子排布规律,可知该元素的原子结构示意图为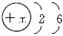 ,在原子中,质子数=核外电子数=8。
,在原子中,质子数=核外电子数=8。
本题难度:简单
5、选择题 目前已知的110多种元素中,形成化合物种类最多的元素是
A.碳
B.氢
C.氧
D.氮
参考答案:A
本题解析:化合物种类最多的是有机化合物,而有机化合物中都含有碳元素,所以形成化合物种类最多的元素是碳,答案选A。
点评:该题是基础性试题的考查,难度不大。属于识记性知识的检验,记住即可。
本题难度:简单