1、选择题 下列说法正确的是(?)
A. H、
H、 H、
H、 H2、H+、H2互为同位素
H2、H+、H2互为同位素
B.C60、金刚石、石墨互为同素异形体
C.H2、D2的性质完全相同
D.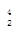 He的最外层电子数为2,所以
He的最外层电子数为2,所以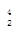 He具有较强的金属性
He具有较强的金属性
参考答案:B
本题解析:质子数相同而中子数不同的同一种元素的不同核素互为同位素,氢气是单质,不是核素,A不正确;由同一种元素形成的不同单质,互称为同素异形体,据此可知选项B正确;H2、D2的物理性质不同,化学性质相似,C不正确;He是稀有气体元素,化学性质稳定,D不正确,答案选B。
点评:该题是基础性试题的考查,侧重对学生基础知识的训练。意在巩固基础,提高能力。该题的关键是明确同位素、同素异形体的含义以及判断依据,并能灵活运用即可,有利于培养学生的逻辑思维能力。
本题难度:一般
2、选择题 X、Y是周期表中的两种元素,X原子的半径比Y的半径小,且具有相同的电子
层数,(选项中m、n均为正整数)下列有关叙述正确的是:
A.若X、Y原子序数相差1,Y为ⅡA族,则X一定是ⅢA族
B.若H n XO m为强酸,则X的氢化物溶液于水一定显酸性
C.若Y元素形成的单质是气体,则X元素形成的单质一定也是气体
D.若Y(OH)m易溶于水,则X(OH)n一定不溶于水
参考答案:C
本题解析:
分析:由题中信息(X原子的半径比Y的半径小,且具有相同的电子层数,)结合元素周期律,推断XY元素在周期表中的位置,然后判断选项的正误.
解:电子层数相等,x原子的半径比y的原子半径小,那么X的核电荷数必然比Y大,所以在周期表中,X的位置在Y的右边.
A 没说是短周期元素,X可能为第IIIB族,故A错误.
B 若X为N元素,氢化物为NH3,其水溶液显碱性,故B错误.
C 同一周期,单质的状态由固态到气态,或由固态到液态再到气态,X的位置在Y的右边,所以,若Y元素形成的单质是气体,则X元素形成的单质一定也是气体,故C正确.
D若Y为K元素,X为Ca 氢氧化钙能溶于水,故D错误.
故选C.
本题难度:简单
3、选择题 下列物质不属于混合物的是
A.漂白粉
B.液氧
C.氯水
D.盐酸
参考答案:B
本题解析:
本题难度:一般
4、选择题 下列物质性质变化规律正确的是?(?)
A.O、F、H的原子半径依次减小
B.HI、HBr、HCl、HF的沸点依次降低
C.干冰、钠、冰的熔点依次降低
D.金属Na、Mg、Al的硬度依次降低
参考答案:A
本题解析:HF分子间存在氢键,HF的沸点高于HI的,B不正确;钠是金属晶体,熔点高于冰的,C不正确;金属Na、Mg、Al的硬度依次升高,D不正确,答案选A。
点评:该题是中等难度的试题,试题贴近高考,注重对学生能力的培养,有利于培养学生的逻辑思维能力。该题的关键是记住常见物质的性质递变规律,然后灵活运用即可。
本题难度:简单
5、选择题 2012年1月,俄美科学家联合小组宣布合成出114号元素的一种同位素, 该同位素原子的质量数为298。以下叙述正确的是(?)
A.该元素属于第六周期
B.该元素位于第ⅢA族
C.该元素为金属元素,性质与82Pb相似
D.该同位素原子含有114个电子,185个中子
参考答案: C
本题解析: A、根据核外电子数排布规律,114号元素位于元素周期表的第七周期、第四主族,错误;B错误;C、该元素与82Pb同主族,在82Pb的下方,是金属元素,性质与82Pb相似 ,正确;D、该同位素原子的质量数为298,质子数是114,则中子数是298-114=184,错误,答案选C。
本题难度:一般