1、选择题 设阿伏加德罗常数的数值为NA,则下列说法正确的是:(?)
A.常温常压下,11.2 L甲烷中含有的氢原子数为2NA
B.标准状况下,0.3 mol二氧化碳中含有氧原子数为0.3 NA
C.常温下,2.7 g铝与足量的盐酸反应,失去的电子数0.3 NA
D.常温下,1 L 0.1 mol / L MgCl2溶液中含Mg2+数为0.2 NA
参考答案:C
本题解析:A错误,非标准状况下的气体摩尔体积题目没有给出,所以无法计算.
B错误,标准状况下,0.3 mol二氧化碳中含有氧原子数为0.6 NA
C正确,铝不足,以铝的量来计算,0.1molAL失去0.3mol电子,数目为0.3 NA
D错误, 1 L 0.1 mol / L MgCl2溶液中含Mg2+数为0.1 NA
本题难度:一般
2、选择题 和2 2 g CO2所含分子数相等的水的质量为(?
2 g CO2所含分子数相等的水的质量为(? )
)
A.44 g
B.22 g
C.18 g
D.9 g
参考答案:D
本题解析:略
本题难度:简单
3、填空题 0.2mol NH3 质量为________,在标准状况下的体积为_______,所含氢原子的物质的量为_______,将其溶于水配制成1L溶液,所得溶液中溶质的物质的量浓度为________。
参考答案:3.4g;4.48L;0.6mol;0.2mol/L
本题解析:
本题难度:简单
4、填空题 制备Cl2需用8mol・L-1的盐酸100 mL,现用12 mol・L-1的盐酸来配制。
(1)需要用量筒量取12 mol・L-1的盐酸的体积为?mL;
(2)实验室提供有如下仪器,为完成配制需要选择的仪器为(填序号)?。
A.100mL量筒? B.托盘天平
C.玻璃棒? D.50mL容量瓶
E.10mL量筒? F.胶头滴管
G.100mL烧杯? H.100mL容量瓶
(3)下列实验操作中,不正确的是?(填写标号)。
A.使用容量瓶前,检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,用量筒量取浓盐酸并沿玻璃棒倒入容量瓶中,缓慢加入蒸馏水到距离刻度线1~2 cm处,改用胶头滴管滴加蒸馏水直到凹液面的最低点和刻度线相平
D.定容后盖好瓶塞,用食指顶住瓶塞,用另一只手托住瓶底,把容量瓶倒转和摇动多次
参考答案:(1)67 mL (2)A、C、F、G、H (3)B、C
本题解析:(1)根据c1V1=c2V2,8 mol・L-1×0.1 L=12 mol・L-1×V,则V=0.0667 L=66.7 mL,用100 mL量筒量取67 mL。
(2)需要的仪器为100 mL量筒、玻璃棒、胶头滴管、100 mL烧杯,100 mL容量瓶。
(3)容量瓶不用待配液润洗,B项错误。浓HCl不能直接倒入容量瓶中,需在烧杯中稀释,C项错误。
本题难度:一般
5、填空题 (6分)某学生为了测定由两种元素形成的气态化合物X的组成,进行了如图所示的实验,将装置内空气排尽后,把气体X由注射器A缓慢送入装有CuO的B装置,使之完全反应(气态化合物X与CuO均无剩余),得到如下结果:
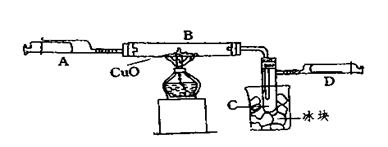
①实验前B管及药品的质量为21.32克,实验后为21.16克
②C管中收集到的物质电解后可得到H2和O2,在D中收集到的是N2。
③X中两元素的质量比是14:3。问:
(1)C中收集到的液体,物质的量是 mol;
(2)在实验中看到的现象是 。
(3)B中反应的化学方程式是 。
参考答案:(1)0.01mol; (2)黑色固体逐渐变为红色;C管中有无色液体出现;D的内管向外推动。
(3)2NH3+3CuO 3Cu十N2↑+3H2O
3Cu十N2↑+3H2O
本题解析:(1)“D中收集到的是N2”,“C管中收集到的物质电解后可得到H2和O2”,根据这两个信息知道X中含有N、H两中元素,C是H2O,又有“X中两元素的质量比是14:3” 则可得氮、氧两种元素的原子个数比为1:3.所以X化学式为NH3; “由实验前B管及药品的质量为21.32g,实验后为21.16g”,可知B管质量减少了0.16g;减少的是O元素的质量,n(O)= 0.16g÷16g/mol="0.01mol" ,则收集到的水的物质的量为0.01mol;(2)根据以上分析知道氧化铜与氨气反应生成铜和水和氮气.所以现象为黑色固体逐渐变为红色,C管中生成水,冷却后变为无色液体,产生氮气,压强增大,注射器的内管向外推动;(3)根据以上分析,反应物为NH3和CuO,生成物为Cu、N2和H2O,则化学方程为:2NH3+3CuO 3Cu十N2↑+3H2O
3Cu十N2↑+3H2O
考点:物质组成的推测、实验现象的描述和物质的量的有关计算。。
本题难度:一般