1、选择题 要证明溴乙烷中溴的存在,下列各操作步骤:①加入AgNO3溶液;②加入NaOH水溶液;③加热;④加入蒸馏水;⑤加稀硝酸至溶液呈酸性;⑥加入NaOH醇溶液。顺序正确且操作最简单,化学药品选用最少的是(? )
A.④③⑤①
B.②③⑤①
C.④⑥③①
D.⑥③⑤①
参考答案:B
本题解析:证明溴乙烷中溴元素的存在,先发生②加入氢氧化钠溶液并③加热,发生水解反应生成NaBr再发生⑤加入稀硝酸至溶液呈酸性,最后①加入硝酸银溶液,生成淡黄色沉淀,则证明含溴元素,即操作顺序为②③⑤①,故选择D。
本题难度:一般
2、选择题 下列物质不能使有色布条褪色的是
A.氯水
B.SO2
C.H2O2溶液
D.氯化钙溶液
参考答案:D
本题解析:分析:具有强氧化的物质具有漂白性,如氯水、HClO、过氧化氢、过氧化钠等,二氧化硫与有色物质化合生成无色物质,也具有漂白性,活性炭具有吸附性能使有色物质褪色,以此来解答.
解答:A.氯水中HClO具有强氧化性、漂白性,能使有色布条褪色,故A不选;
B.二氧化硫与有色物质化合生成无色物质,能使有色布条褪色,故B不选;
C.H2O2溶液具有强氧化性、漂白性,能使有色布条褪色,故C不选;
D.氯化钙溶液不具有强氧化性、漂白性,则不能使有色布条褪色,故D选;
故选D.
点评:本题考查漂白性,注意归纳常见的具有漂白性的物质及其漂白原理,明确物质的性质即可解答,题目难度不大.
本题难度:简单
3、填空题 (8分)卤代烃在生产生活中具有广泛的应用,回答下列问题:
(1)多卤代甲烷作为溶剂,其中分子结构为正四面体的是__________。工业上分离这些多卤代甲烷的方法是_______________________。
(2)三氟氯溴乙烷(CF3CHClBr)是一种麻醉剂,写出其所有同分异构体的结构简式__________(不考虑立体异构)。
(3)聚氯乙烯是生活中常见的塑料。工业生产聚氯乙烯的一种工艺路线如下:
反应①的化学方程式是_____________,反应类型为_______,反应②的反应类型为___________。
参考答案:(1)四氯化碳?分馏(2)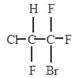 、
、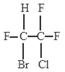 、
、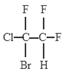 ?
?
(3)H2C=CH2+Cl2→CH2ClCH2Cl?加成反应?消去反应
本题解析:(1)甲烷是正正四面体结构,若分子中的四个H原子全部被Cl原子取代得到CCl4,还是有极性键构成的非极性分子。由于这些多卤代甲烷都是分子晶体构成的物质,沸点不同,因此可采取分馏的方法分离。(2)三氟氯溴乙烷(CF3CHClBr)是一种麻醉剂,其所有同分异构体的结构简式是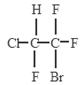 ;
;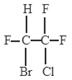 ;
;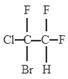 。(3)乙烯与氯气发生加成反应得到1,2-二氯乙烷;反应①的化学方程式是H2C=CH2+Cl2→CH2ClCH2Cl。1,2-二氯乙烷在480℃~530℃条件下发生消去反应得到氯乙烯CH2="CHCl." 氯乙烯发生加聚反应得到聚氯乙烯。
。(3)乙烯与氯气发生加成反应得到1,2-二氯乙烷;反应①的化学方程式是H2C=CH2+Cl2→CH2ClCH2Cl。1,2-二氯乙烷在480℃~530℃条件下发生消去反应得到氯乙烯CH2="CHCl." 氯乙烯发生加聚反应得到聚氯乙烯。
本题难度:一般
4、选择题 下列卤代烃在KOH醇溶液中加热不反应的是( )
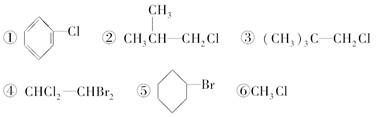
A.①③⑥
B.②③⑤
C.全部
D.②④
参考答案:A
本题解析:卤代烃在KOH醇溶液中加热可发生消去反应的前提:邻位碳原子上有氢原子。
本题难度:一般
5、实验题 (12分)学习卤代烃性质时,我们知道溴乙烷在不同溶剂中与氢氧化钠发生不同类型的反应,生成不同的反应产物。我们可以通过实验的方法去验证反应的产物:
(1)在溴乙烷与氢氧化钠的乙醇溶液的?(反应类型)中可以观察到有气体生成。某同学用如下图所示装置对该气体进行验证,他所观察到的现象是?;
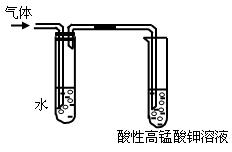
(2)盛水试管的作用是?;
(3)除了用酸性高锰酸钾溶液外,还可以用?试剂检验该气体,其反应原理是?(用化学方程式表示)。
(4)另一位同学取少量溴乙烷与氢氧化钠水溶液反应后的混合溶液,向其中滴加硝酸银溶液,加热,产生少量沉淀。该同学由此得出溴乙烷与氢氧化钠水溶液反应,生成了溴化钠。老师和同学都认为这样不合理。若请你用实验验证该反应中生成了溴化钠,你与该同学实验方案不同的实验方法是?。
参考答案:(12分)(1)消去反应?高锰酸钾褪色
(2)除去气体中少量的乙醇
(3)溴水? CH2==CH2 + Br2 → BrCH2CH2Br
(4)将混合溶液先用稀硝酸酸化,再向溴乙烷中加硝酸银溶液
本题解析:略
本题难度:一般