若沉淀中出现绿色的迹象,则假设二成立;
若沉淀中没有出现任何绿色的迹象,则假设二不成立。
参考答案:6Fe(OH)2+O2+2H2O==2Fe3(OH)8 (2分)
假设二:绿色物质是Fe3(OH)8 (2分)
(1)铁粉、稀硫酸(2分)(2)三、一(2分)
(3)(4分)②迅速用长滴管伸入液面下依次挤入一滴饱和FeSO4 溶液、一滴NaOH溶液
③将O2缓缓通入白色沉淀中
本题解析:氢氧化亚铁不稳定,极易被氧化,方程式为6Fe(OH)2+O2+2H2O==2Fe3(OH)8。
根据已知信息可知,假设二应该是绿色物质是Fe3(OH)8 。
(1)硫酸亚铁极易被氧化,生成硫酸铁,所以为防止氧化,应该加入铁粉;同时硫酸亚铁还易水解,溶液显酸性,因此还要加入稀硫酸防止水解。
(2)实验一与实验三相比,不同是温度,温度高溶解度,如果降低温度则会析出晶体,所以根据实验一与实验三现象可知,假设一是正确的。
(3)②是制取氢氧化亚铁,所以正确的操作是迅速用长滴管伸入液面下依次挤入一滴饱和FeSO4 溶液、一滴NaOH溶液。
③假设二是由于被氧化而导致的,所以正确的操作是将O2缓缓通入白色沉淀中。
本题难度:一般
3、选择题 用足量的CO还原32.0g某种氧化物,将生成的气体通入足量澄清石灰水中,得到60g沉淀,则该氧化物是
A.FeO
B.Fe2O3
C.CuO
D.Cu2O
参考答案:B
本题解析:
解:由关系式C0 ~CaCO3得,n(CaCO3)=60g/100g・mol-1=0.6mol=n(CO)
0.6molCO能还原A、72g/mol×0.6mol=43.2g;B、160 g/mol×0.6mol/3=32.0g符合题意;C、80 g/mol×0.6mol=48.0g;D、144 g/mol×0.6mol=86.4g
综上所述,正确答案为D
本题难度:一般
4、选择题 硫酸亚铁是一种重要的化工原料,可以制备一系列物质(如下图所示)。下列说法错误的是( )
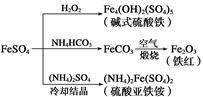
A.碱式硫酸铁水解能产生Fe(OH)3胶体,可用作净水剂
B.为防止NH4HCO3分解,生产FeCO3需在较低温度下进行
C.可用KSCN溶液检验(NH4)2Fe(SO4)2是否被氧化
D.常温下,(NH4)2Fe(SO4)2在水中的溶解度比FeSO4的大
参考答案:D
本题解析:A项,Fe3++3H2O Fe(OH)3(胶体)+3H+;B项,NH4HCO3加热很容易分解,所以制备FeCO3需低温下进行;C项,SCN-可以检验微量Fe3+;D项,FeSO4和(NH4)2SO4冷却时会结晶析出(NH4)2Fe(SO4)2,所以(NH4)2Fe(SO4)2的溶解度较小。 Fe(OH)3(胶体)+3H+;B项,NH4HCO3加热很容易分解,所以制备FeCO3需低温下进行;C项,SCN-可以检验微量Fe3+;D项,FeSO4和(NH4)2SO4冷却时会结晶析出(NH4)2Fe(SO4)2,所以(NH4)2Fe(SO4)2的溶解度较小。
本题难度:一般
5、实验题 (12分)
实验室用下面装置测定FeO和Fe2O3固体混合物中Fe2O3的质量,D装置的硬质双通玻璃管中的固体物质是FeO和Fe2O3的混合物。
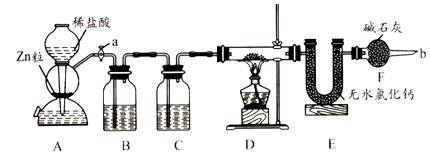
(1)如何检查装置A的气密性?
(2)为了安全,在点燃D处的酒精灯之前,在b处必须?。
(3)装置B的作用是?
装置C中装的液体是?
(4)在气密性完好,并且进行了必要的安全操作后,点燃D处的酒精灯,在硬质双通玻璃管中发生的化学反应方程式是??
(5)若FeO和Fe2O3固体混合物的质量为23. 2g,反应完全后,U型管的质量增加7.2g则混合物中Fe2O3的质量为?_。
参考答案:(12分)
(1)开启旋塞,向长颈漏斗中加水。当水充满容器下部的半球体时,关闭旋塞。继续加水,使水上升到长颈漏斗中。静置片刻,若水面不下降,则说明装置气密性良好
(2)验纯
(3)除HCl、浓H2SO4
(4)Fe2O3+3H2=2Fe+3H2O? FeO+H2=Fe+H2O
(5)16g
本题解析:考查了气体的制取和物质的测定的相关实验操作
(3)装置B、C为气体的净化装置,分别除去氢气里的HCl及水蒸汽。
(4)根据混合物的质量及产物水的质量列出方程组计算即可。
本题难度:一般
|