1��ѡ���� ijЩ�������ijɷ��к����������������ڷ��û������������ʡ��������������Ƿ���ʵ��Լ���
A��ϡ����
B��KSCN��Һ
C����ˮ
D������
�ο��𰸣�B
���������Fe2+�������е���������ΪFe3+��Fe3+�ļ��鷽���������Һ�еμ�KSCN��Һ������ΪѪ��ɫ��Һ����֤������Fe3+����Ӧ�����ӷ���ʽΪ��Fe3++3SCN-=" Fe" (SCN)3.ѡ��ΪB.3+�ļ��鷽����
�����Ѷȣ���
2��ʵ���� ʵ�������ú�����CO2���ʵ�CO����ԭ����������FexOy��֤��CO�ܹ���ԭFexOy���ұ���������ΪCO2��ʵ�����ṩ�ĸ���������ҩƷ���£�
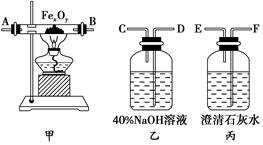
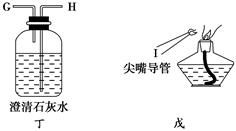
(1)ʵ��ʱ����������װ�õ���ȷ����˳����(��д���ӿڵĴ���)���������D��________��________��(F)��(E)��________��________��________��________��________��
(2)��װ�����з�����Ӧ�Ļ�ѧ����ʽ��_______________________��
(3)��װ�ü��з�����Ӧ�Ļ�ѧ����ʽ��______________��
(4)��װ���г���ʯ��ˮ��������_______________��
(5)�������ⶨ��0.4 g FexOy��CO��Ӧ���ɵ�����ͨ������ij���ʯ��ˮ�У�����0.75 g��ɫ��������FexOy��xֵ��________��yֵ��________��
(6)ʵ������У���˵��CO�ܹ���ԭFexOy��ʵ��������___________���ܹ�˵��CO��������CO2��ʵ��������____________��
�ο��𰸣�(1)D��C��A��B��H��G��I
(2)2NaOH��CO2=Na2CO3��H2O
(3)FexOy��yCO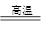 xFe��yCO2
xFe��yCO2
(4)����CO2�Ƿ����
(5)2��3
(6)�����ĩ�Ӻ�ɫ���ɫ�����г���ʯ��ˮ�����
�����������ʵ��Ŀ�ģ�����ÿ��װ�õ����ã�Ȼ�����ӣ�x��yֵ�ļ�������C�غ��ϵCO��CO2��CaCO3
n(CaCO3)��n(CO)��0.75/100��7.5��10��3mol
FexOy����������Ϊ44 g��mol��1��7.5��10��3mol��28 g��mol��1��7.5��10��3mol��0.12 g
n(Fe)��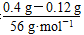 ��0.005 mol��
��0.005 mol��
n(O)��0.12/16��0.007 5 mol��
x/y��2/3
�����Ѷȣ�һ��
3������� ������һ����Ҫ�����ϣ���ѧʽΪFe2O3��xH2 O���㷺����Ϳ�ϡ������ϡ��Ľ���Ʒ�ȹ�ҵ��ʵ����ģ�ҵ����������(��FeZ 0����������CaO, Mg0��)�ͻ������
(��Ҫ�ɷ�ΪFeS2)�Ʊ����Ƶ���������:
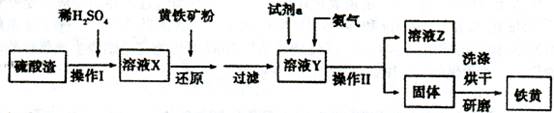
��1������I�����II�ж��õ��������������������ֲ����е����÷ֱ���_?��?
��2���Լ�a���ѡ��_?(��ѡ��ʹ�õ���:���ۡ�������ŨHNO3 );��������_?��
��3���������������õ�����������װ�ÿ�����ʵ�����ư�������_?_(�����)��
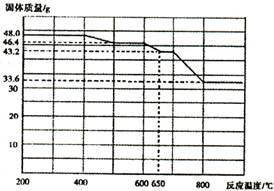
��4����������֪���ڲ�ͬ�¶���Fe2 O3��CO��ԭ���������ΪFe3 O4?��FeO��Fe�����������뷴Ӧ�¶ȵĹ�ϵ����ͼ��ʾ������ͼ���ƶ�670��ʱFe2 O3��ԭ����Ļ�ѧʽΪM�������һ����ʵ�飬֤���û�ԭ����ijɷ�(������дÿ�������������Լ��Ļ�ѧʽ������ͽ���)��������ѡ���ɹ�ѡ����Լ�:ϡH2SO4��ϡ���ᡢH2 O2��Һ��NaOH��Һ��KSCN��Һ��
�����Լ�
| ����
| ����
|
?
| ?
| ��ԭ����Ϊ?
|
?
| ?
|
?
| ?
|
?
�ο��𰸣�
��1�����������Һ����������2����������������������������������Ϊ���������ӣ���3��bd; ��4��
�����Լ�
����
����
ϡ�����ϡ����
������ȫ�ܽ��������ݲ���
��ԭ����ΪFeO?
KSCN��Һ
��Һ����ɫ
H2O2��Һ
��Һ��Ϊ��ɫ
�����������1������I�ǽ��������Һ�ܽ⣬����II�ǹ��˲�������Ҫ�õ���������������2���Լ�a���ѡ�ÿ�������Դ���ۣ�����������������������������������Ϊ���������ӡ���3��ʵ�����ư�������Ҫ�Dz������������㣬���ڰ���������ˮ����Ҫ���ȣ���ѡ��bd����4�����ڶ���������������KSCN��Һ���Ժ�ɫ�жϣ����������������ü������������������жϡ�CO��ԭ�������Ļ�ԭ����Ϊ����Fe3O4��FeO��Fe��Fe2O3�����¶ȿɴﵽ500�桫600�棬������46.4g����Ϊ45g����ԭ����ΪFe3O4��650�桫700��ʱ��������43.2g���ٽϴ�ԭ����ΪFeO��Ϊ��֤��ԭ����������������м���ϡH2SO4����ȫ�ܽ⣬�ټ����������������Һ����Һ��ɫ��ȥ����˵����ԭ����ΪFeO���ʴ�Ϊ��Fe3O4���������������м���ϡH2SO4����ȫ�ܽ⣬�ټ����������������Һ����Һ��ɫ��ȥ��
�����Լ�
����
����
ϡ�����ϡ����
������ȫ�ܽ��������ݲ���
��ԭ����ΪFeO?
KSCN��Һ
��Һ����ɫ
H2O2��Һ
��Һ��Ϊ��ɫ
���㣺
�����Ѷȣ�����
4�������� ��������ͭ��ɵĺϽ�a mol������ͭ�����ʵ�������Ϊx�����˺Ͻ��гɷ�ĩ״��ȫ��Ͷ�뺬b mol�����ϡ��Һ�У���ʹ���ַ�Ӧ������Ļ�ԭ����ֻ��NO��
��1�������ӷ�����д���пհף��оٳ�ȫ�����ܳ��ֵ��������
��2������Һ�н�������ֻ��Fe2+��Cu2+ʱ����b��ȡֵ��ΧΪ����a��x��ʾ��
��3����x=0��5ʱ����Һ��Fe3+�� Fe2+�����ʵ�����ȣ��ڱ�״���¹�����672����NO���壬��a��b��ֵ��
�ο��𰸣���1��
?����
��?��
��
��
��
��
��
��
��������ɷ�
Fe��Cu
Cu
Cu
��
��
��
��Һ �н�������
�������
Fe2��
Fe2��
Fe2��[��]
Cu2��
Fe2��
Cu2��
Fe2����Cu2��Fe3��
Fe3��
Cu2��m]
�����������
�����Ѷȣ�һ��
5��ѡ���� ����һ��Ӧ�ù㷺�Ľ����������й�����˵����ȷ����
A���������ᷴӦ�����Ȼ���������
B������������Ũ�����жۻ�
C������������ȼ��������Ϊ����������
D����������״���Ǻ�ɫ����
�ο��𰸣�B
������������������ᷴӦ�����Ȼ�������������A����ȷ��B��ȷ��C����ȷ������������ȼ����������������������������ɫ������D����ȷ����ѡB��
������������ʶ����֪ʶ�Ŀ��飬�ѶȲ���ƽʱע��֪ʶ�Ļ��ۺ��ܽᣬ����������ü��ɣ������ڹ��̻�����ͨ��ѧ����Ӧ��������
�����Ѷȣ�һ��