1��ѡ���� ���и����ڵ�����Ԫ�أ��ڽ����Ի�ǽ����Է������������Ե���
A.������
B.�ƺ���
C.þ����
D.�غͷ�
�ο��𰸣�A
����������ơ�þ�ͼض��ǵ��͵Ľ���Ԫ�أ��⡢���������ȶ��ǵ��͵ķǽ���Ԫ�أ���Ԫ�ؼ��н��������зǽ����ԣ��ʴ�ΪA��
�����Ѷȣ�һ��
2������� �±��������Ԫ�����ڱ���һ����Ԫ�أ��ش���������
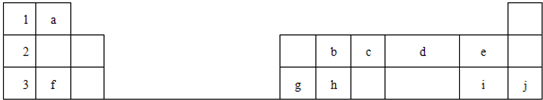
��1�������г���10��Ԫ���У���ѧ��������õ���______����Ԫ�����ƣ���ͬ�����ǽ�������ǿ����______��ԭ�Ӱ뾶��С����______��
��2������bd2�ĵ���ʽ______��Ԫ��e�ĸ�һ�������ӵĽṹʾ��ͼ______��
��3������bd2��hd2���������������ž���죬��ԭ��������bd2����______���壬����hd2����______���壮
��4��Ԫ��e����̬�⻯���Ԫ��i����̬�⻯��______����ȶ������ȶ�����
��5��Ԫ��f��g������������Ӧˮ����֮�䷴Ӧ�����ӷ���ʽ��______��
��6������fda���еĻ�ѧ��������______��
�ο��𰸣�����Ԫ�������ڱ��еķֲ�֪ʶ������ȷ��a��H��b��C��c��N��d��O��e��F��f��Na��g��Al��h��Si��i��Cl��j��Ar��
��1�������г���10��Ԫ���У�ϡ������Ԫ��Ar��ѧ�����ȶ���ͬһ���ڣ�Ԫ��ԭ�Ӱ뾶�����Ұ뾶�ڼ�С��ͬһ����Ԫ�ص�ԭ�Ӱ뾶���ϵ�������������ԭ�Ӱ뾶��С����H��ͬ����Ԫ�ص�ԭ�Ӵ����ң�Ԫ�صķǽ���������ǿ��ͬһ���壬Ԫ�ص�ԭ�Ӵ��ϵ��£�Ԫ�صķǽ��������������Էѽ�������ǿ����F���ʴ�Ϊ��벣������⣻
��2��������̼��̼ԭ�Ӻ���ԭ��֮��ͨ������˫���γɵĹ��ۻ��������ʽΪ��
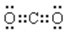
�������Ӻ��������Ϊ10�����ӵĽṹʾ��ͼΪ��
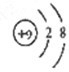
���ʴ�Ϊ��
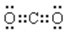
��

��
��3��������̼�Ƿ��Ӿ��壬����������ԭ�Ӿ��壬���Ӿ�����۵����ԭ�Ӿ��壬�ʴ�Ϊ�����ӣ�ԭ�ӣ�
��4��ͬ����Ԫ�ص�ԭ�ӣ����ϵ����⻯��Խ��Խ�ȶ�������Ԫ��F����̬�⻯���Ԫ��Cl����̬�⻯���ȶ����ʴ�Ϊ���ȶ���
��5��Ԫ��f������������Ӧˮ�������������ƣ�g������������Ӧˮ��������������������������������������ܺ�ǿ�Ӧ��ʵ���ǣ�Al��OH��3+OH-=[Al��OH��4]-���ʴ�Ϊ��Al��OH��3+OH-=[Al��OH��4]-��
��6�����������������Ӻ�������֮�������Ӽ���������֮���ǹ��ۼ����ʴ�Ϊ�����Ӽ����ۼ���
���������
�����Ѷȣ�һ��
3��ѡ���� ij�����ڷǽ���Ԫ�ص�ԭ�Ӻ��������������Ǵ�����������һ�룬��Ԫ��
[? ]
A������Ȼ����ֻ�Ի���̬����
B�����ʳ������뵼����Ϻ��ά
C����������ﲻ���ᷴӦ
D����̬�⻯��ȼ����ȶ�
�ο��𰸣�A
���������
�����Ѷȣ���
4��ѡ���� A��B��ǰ������Ԫ�أ����ǵ�����A2-��B3+������ͬ�ĺ�����Ӳ�ṹ������˵������ȷ����
A.ԭ������A��B
B.ԭ�Ӱ뾶A��B
C.���Ӱ뾶A2-��B3+
D.������ΪA��B
�ο��𰸣�C
��������������ӵĽṹ��ϵ��֪B��A����һ���ڣ�ԭ������B��A��ԭ�Ӱ뾶B��A�����Ӱ뾶A2-��B3+��������Ӧ��B��A��
�����Ѷȣ���
5������� �±���Ԫ�����ڱ���һ���֣�
��
���� | I?A | II?A | III?A | IV?A | V?A | VI?A | VII?A
һ
|
��
a
b
?d
e
��
f
g
h
j
|
��1������Ԫ�صĵ������۵���ߵĿ�����______����Ԫ�ط��ţ���д��a���Ȼ���ĵ���ʽ______��e��f��h�γɵļ����ӵİ뾶�ɴ�С˳������Ϊ______�������ӷ��ţ���
��2����һ�������£�j��d���γ�һ�ֻ����������Ϊ����ɫҺ�壬���侧������Ϊ______����������ˮǿ��ˮ�⣬�������ֲ������֮һ�ķ��ӹ���Ϊ�����Σ���һ�����ʾ���Ư���ԣ�д����ط�Ӧ�Ļ�ѧ����ʽ______��
��3������һ��Ԫ�أ���ԭ�ӻ��һ���������ͷų��������ϱ�������Ԫ�������ģ���Ԫ���DZ���______Ԫ�أ����ţ���
��4����g�ĵ���������f���ʣ��γ�����k����g��f��k��Ӳ��������______�����������ƣ���
��5�����Ƶ�117��Ԫ�أ���Ԫ�����ڱ��н�����ǽ����ķ�������Ӧ��һ��______��ѡ����������ǽ�������Ԫ�أ�д��117��Ԫ�����������Ų�ʽ______��
��6�����ö�����Ԫ�أ�д����������ԭ���ӻ�������Ͳ�ͬ��AB3�ͷ��ӵĻ�ѧʽ______��______��
�ο��𰸣���Ԫ�������ڱ���λ�ÿ�֪aΪLiԪ�أ�bΪCԪ�أ�dΪNԪ�أ�eΪFԪ�أ�fΪMgԪ�أ�gΪAlԪ�أ�hΪSԪ�أ�jΪClԪ�أ�
��1��̼���ʴ���ԭ�Ӿ��壬��̼Ԫ�ص����۵������ߣ��Ȼ����������������ӹ��ɣ�����ʽΪ
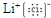
�����Ӳ�ṹ��ͬ���˵����Խ�����Ӱ뾶ԽС���������Ӱ뾶F-��Mg2+��������������ͬ�����Ӳ�Խ�����Ӱ뾶Խ���������Ӱ뾶S2-��F-���������Ӱ뾶S2-��F-��Mg2+��
�ʴ𰸣�C��
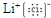
��S2-��F-��Mg2+��
��2��j��d�γɻ�������NCl3��������Ϊ����ɫҺ�壬�е�ϵͣ����ڷ��Ӿ��壮NCl3��ˮǿ��ˮ�⣬�������ֲ������֮һ�ķ��ӹ���Ϊ������ΪNH3����һ�����ʾ���Ư������HClO����Ӧ����ʽΪNCl3+3?H2O�TNH3+3HClO��
�ʴ�Ϊ��NCl3+3?H2O�TNH3+3HClO��
��3��ͬ����������ң��縺������ͬ�������϶��£��縺�Լ�С�����Ե縺�������FԪ�أ�Fԭ�ӻ��һ���������ͷų�������࣬�ʴ�Ϊ��e��
��4���Ͻ��Ӳ�ȸ��ڸ���֣�������þ�Ͻ�Ӳ����ʴ�Ϊ����þ�Ͻ�
��5����������0��Ԫ��Ϊ118�ţ�����117��Ԫ�ش��ڵ������ڵڢ�A�壬���������Ų�ʽΪ7s27p5�������������ܵ��Ӳ��������ڽ���Ԫ�أ�
�ʴ�Ϊ��������7s27p5��
��6��AB3�ͷ��ӿ���Ϊ�����ͣ���NH3��Nԭ�Ӳ�ȡsp3�ӻ���Ҳ������ƽ�������Σ���BF3��Bԭ�Ӳ�ȡsp2�ӻ����ʴ�Ϊ��NH3��BF3��
���������
�����Ѷȣ�һ��