1、选择题 红热的炭和水蒸气反应生成1mol氢气和1mol一氧化碳气体,吸收131.3KJ热量.能表示该反应热化学方程式的是( )
A.C+H2O→H2+CO-131.3KJ
B.C(s)+H2O(l)→H2(g)+CO(g)+131.3KJ
C.C(s)+H2O(g)→H2(g)+CO(g)+131.3KJ
D.C(s)+H2O(g)→H2(g)+CO(g)-131.3KJ
参考答案:D
本题解析:
本题难度:一般
2、填空题 (16分)
用CaSO4代替O2与燃料CO反应,既可提高燃烧效率,又能得到高纯CO2,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。
1/4CaSO4(s)+CO(g) ? 1/4CaS(s)+CO2(g) ?H1 = -47.3kJ?mol-1
② CaSO4(s)+CO(g) ? CaO(s)+CO2(g) +SO2(g) ?H2 = +210.5kJ?mol-1
③ CO(g) ? 1/2C(s)+1/2CO2(g) ?H3 = -86.2kJ?mol-1
(1)反应2CaSO4(s)+7CO(g) ? CaS(s)+ CaO(s)+6CO2(g)+ C(s) +SO2(g)
的?H=__________(用?H1、?H2和?H3表示)
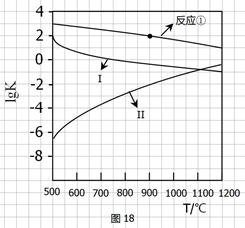
(2)反应①-③的平衡常数的对数lgK随反应温度T的变化曲线见图18,结合各反应的?H,回答下列问题。a)曲线中对应反应②的是_______(选填“Ⅰ”或“Ⅱ”)。
归纳lgK-T曲线变化规律: b)_________ ________ 。
c)_____ ___ 。
(3)向盛有CaSO4的真空恒容密闭容器中充入初始浓度为C0 mol?L-1的CO,反应①于900℃
达到平衡,此时c平衡(CO)=8.0X10-5 mol?L-1。
d)用图18中相应的lgK的值计算CO的转化率(忽略副反应,计算结果保留两位有效数字)。
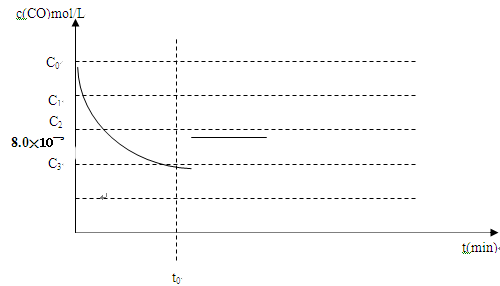
e) c(CO)随反应时间t的变化曲线如图19所示。
若保持其他条件不变,请在答题卡坐标图中分别画出升高反应温度(高于900℃)和降低反应温度(低于900℃)c(CO)随反应时间t的变化曲线图,并作相应的标注(忽略副反应)。
参考答案:(1)4?H1+?H2+2?H3(2分)(2)a)Ⅱ(2分)
b)当?H>0时,lgK随温度升高而增大(1分),当?H<0时,lgK随温度升高而减小(1分)。其他合理答案也给分
c) 当温度同等变化时,?H的数值越大lgK的变化越大或?H的数值越大lgK受温度的影响越大或放热越多,lgK受温度的影响越大(2分)。其他合理答案也给分
(3)d)α(CO)=99%(4分)e)
本题解析:(1)①×4+②+③×2,整理可得:2CaSO4(s)+7CO(g) ? CaS(s)+ CaO(s)+6CO2(g)+ C(s) +SO2(g)
?H=4?H1+?H2+2?H3;(2)a)由于温度升高,曲线中lgK随温度升高而增大,说明升高温度,平衡正向移动,正反应是吸热反应,?H>0则对应反应②的是Ⅱ;归纳lgK-T曲线变化规律: b) 当?H>0时,lgK随温度升高而增大(1分),当?H<0时,lgK随温度升高而减小(1分)。
c) 当温度同等变化时,?H的数值越大lgK的变化越大或?H的数值越大lgK受温度的影响越大或放热越多,lgK受温度的影响越大(2分)。(3)d)
1/4CaSO4(s)+CO(g)  1/4CaS(s)+CO2(g)
1/4CaS(s)+CO2(g)
初始浓度(mol/L) C0 0
转化浓度(mol/L) C0 ― 8.0X10-5 C0 ― 8.0X10-5
平衡浓度(mol/L) 8.0X10-5 C0 ― 8.0X10-5(1分)
K=" c(" CO2 )/ (c(CO)=100(1分),解得:C0=808×10-5(1分)所以α(CO)=99%(1分)
e)由于2CaSO4(s)+7CO(g) ? CaS(s)+ CaO(s)+6CO2(g)+ C(s) +SO2(g) ?H=4?H1+?H2+2?H3=-151.1KJ/mol;
该反应的正反应是放热反应,升高温度,根据平衡移动原理:化学平衡向吸热反应反应方向移动,对该反应来说,平衡逆向移动,CO的浓度增大;降低温度,平衡正向移动,CO的浓度减小。所以画出图像表示为: 。
。
考点:考查盖斯定律的应用、热化学方程式的书写、化学平衡常数的计算、温度对物质平衡浓度影响的图像法表示的知识。
本题难度:困难
3、填空题 (14)A、B、C、D、E、F是常见单质,其中A是用量最大,应用最广泛的金属;元素D是地壳中含量最多的金属元素;D元素和E元素在周期表中相邻。G、H、I、J、K、L是常见化合物,其中G在常温下是无色液体,H是黑色固体。以上物质相互间的转化关系如图所示:

请回答下列问题:
(1)元素A在元素周期表中的位置为 周期 族。
(2)写出K的电子式 。
(3)写出H和D反应的化学方程式 。
(4)D能与氢氧化钠溶液反应,请写出该反应的离子方程式 。
(5)写出A与G反应的化学方程式 。
(6)K与E反应时产生的现象有 ;该反应的化学方程式为 ___________________。
(7)已知F的燃烧热为akJ/mol,L的燃烧热为bkJ/mol,试写出F生成L的热化学方程式_________________
参考答案:(1)四;VIII ;(2)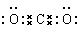 ;(3)3Fe3O4+8Al
;(3)3Fe3O4+8Al 4Al2O3+9Fe
4Al2O3+9Fe
(4)2Al+2OH-+2H2O==2AlO2-+3H2↑ (5)3Fe+4H2O(g) Fe3O4+4H2↑
Fe3O4+4H2↑
(6)镁带剧烈燃烧,放出耀眼的光,瓶壁出现白色固体和黑色颗粒;2Mg+CO2 2MgO+C
2MgO+C
(7) C(s)+ 1/2O2(g) CO (g) ΔH=-(a-b)kJ/mol;
CO (g) ΔH=-(a-b)kJ/mol;
本题解析:根据题意及物质间的转化关系可得:A是Fe;B是H2;C是O2;D是Al;E是Mg;F是C;G是H2O;H是Fe3O4;I是Al2O3;J是MgO;K是CO2;L是CO。(1)26号元素Fe在元素周期表中位于第四周期第VIII族;(2)CO2的电子式是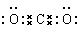 ;(3)Fe3O4和Al发生铝热反应的化学反应方程式是3Fe3O4+8Al
;(3)Fe3O4和Al发生铝热反应的化学反应方程式是3Fe3O4+8Al 4Al2O3+9Fe;(4)Al与氢氧化钠溶液反应的离子方程式是2Al+2OH- +2H2O= 2AlO2- +3H2↑;(5)炽热的Fe与水蒸气反应的化学方程式是3Fe+4H2O(g)
4Al2O3+9Fe;(4)Al与氢氧化钠溶液反应的离子方程式是2Al+2OH- +2H2O= 2AlO2- +3H2↑;(5)炽热的Fe与水蒸气反应的化学方程式是3Fe+4H2O(g) Fe3O4+4H2;(6)Mg带在CO2中能够着火剧烈燃烧,放出耀眼的光,瓶壁出现白色固体和黑色颗粒;反应的化学方程式为2Mg+CO2
Fe3O4+4H2;(6)Mg带在CO2中能够着火剧烈燃烧,放出耀眼的光,瓶壁出现白色固体和黑色颗粒;反应的化学方程式为2Mg+CO2 2MgO+C;(7)根据题意可得热化学方程式①C(s)+ O2(g)
2MgO+C;(7)根据题意可得热化学方程式①C(s)+ O2(g) CO2(g) ΔH="-akJ/mol;" ②CO(g)+ 1/2O2(g)
CO2(g) ΔH="-akJ/mol;" ②CO(g)+ 1/2O2(g) CO2(g) ΔH="-bkJ/mol" bkJ/mol, ①-②整理可得:C(s)+ 1/2O2(g)
CO2(g) ΔH="-bkJ/mol" bkJ/mol, ①-②整理可得:C(s)+ 1/2O2(g) CO (g) ΔH=-(a-b)kJ/mol;
CO (g) ΔH=-(a-b)kJ/mol;
考点:考查元素及化合物的推断、电子式、化学方程式、离子方程式及热化学方程式的书写的知识。
本题难度:困难
4、简答题 (1)已知H2O(l)=H2O(g);△H=+44KJ/mol.在25℃、101kPa下,1g甲醇燃烧生成CO2和气态水时放热19.93kJ,则该反应的热化学方程式应为______.
(2)已知H2的燃烧热△H=-285.8kJ?mol-1,CO的燃烧热△H=-282.8kJ?mol-1.现有CO、H2、CO2组成的混合气体67.2L(标准状况),经充分燃烧后放出的总热量为710.0kJ,并生成18g液态水,求燃烧前混合气体中CO的体积分数.______.
参考答案:(1)由1gCH3OH燃烧放热22.7kJ,则2molCH3OH燃烧放热19,93×32×2=1275.52kJ,则该燃烧反应的热化学方程式为2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g)△H=-1275.52kJ/mol,
故答案为:2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g)△H=-1275.52kJ/mol;
(2)已知H2的燃烧热△H=-285.8kJ?mol-1,热化学方程式为:H2(g)+12O2(g)=H2O(l)△H=-285.58KJ/mol,;
CO的燃烧热△H=-282.8kJ?mol-1.热化学方程式为:CO(g)+12O2(g)=CO2(g)△H=-282.8KJ/mol;现有CO、H2、CO2组成的混合气体67.2L(标准状况)物质的量=67.2L22.4L/mol=3mol,经充分燃烧后放出的总热量为710.0kJ,并生成18g液态水物质的量为1mol,放热为285.58KJ,则一氧化碳燃烧放热=710.0kJ-285.58KJ=424.42KJ,依据热化学方程式计算得到一氧化碳物质的量=1mol×424,42KJ282.8KJ=1.5mol,一氧化碳的体积分数即为物质的量的分数=1.5mol3mol×100%=50%;
故答案为:50%
本题解析:
本题难度:简单
5、填空题 (1)已知:H2(g)+O2(g) H2O(g),反应过程中能量变化如图所示,则:
H2O(g),反应过程中能量变化如图所示,则:

①a、b、c分别代表什么意义?
a ;
b ;
c 。
②该反应是 反应(填“吸热”或“放热”),ΔH
反应(填“吸热”或“放热”),ΔH 0(填“>”或“<”)。
0(填“>”或“<”)。
(2)发射“天宫”一号的火箭使用的推进剂是液氢和液氧,这种推进剂的优点是 , 。(请写两条)
(3)已知:H2(g)+O2(g) H2O(l) ΔH=-285.8 kJ・mol-1
H2O(l) ΔH=-285.8 kJ・mol-1
H2(g) H2(l) ΔH=-0.92 kJ・mol-1
H2(l) ΔH=-0.92 kJ・mol-1
O2(g) O2(l) ΔH=-6.84 kJ・mol-1
O2(l) ΔH=-6.84 kJ・mol-1
H2O(l) H2O(g) ΔH=+44.0 kJ・mol-1
H2O(g) ΔH=+44.0 kJ・mol-1
请写出液氢和液氧生成气态水的热化学方程式: 。
参考答案:(1)①1 mol H2分裂为H、0.5 mol O2分裂为O时吸收的热量 H、O结合生成1 mol H2O(g)放出的热量 1 mol H2和0.5 mol O2生成1 mol H2O(g)时,反应放出的热量
②放热 <
(2)相同质量时,氢气放出的热量多 产物为水,无污染(其他合理答案均可)
(3)H2(l)+O2(l) H2O(g) ΔH=-237.46 kJ・mol-1
H2O(g) ΔH=-237.46 kJ・mol-1
本题解析:(1)化学反应是旧键断裂(吸热)和新键生成(放热)的过程。该反应是吸热还是放热要看这两个过程中能量变化的相对大小。
(3)根据题中所给数据,可求出H2(l)+O2(l) H2O(g)的焓变ΔH的数值,ΔH=(-285.8+0.92+×6.84+44.0) kJ・mol-1=-237.46 kJ・mol-1。
H2O(g)的焓变ΔH的数值,ΔH=(-285.8+0.92+×6.84+44.0) kJ・mol-1=-237.46 kJ・mol-1。
考点:化学反应与能量
本题难度:一般