1、简答题 从化工厂铬渣中提取硫酸钠的工艺如下:
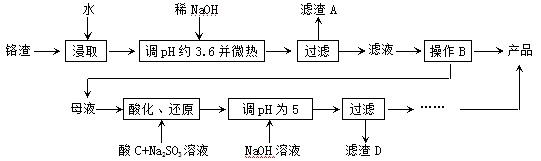
已知:①铬渣含有Na2SO4及少量Cr2O72-、Fe3+;②Fe3+、 Cr3+完全沉淀(c ≤1.0×10-5mol・L-1)时pH分别为3.6和5。
(1)“微热”除能加快反应速率外,同时还可以?,滤渣A为?(填化学
式)。
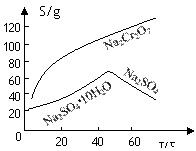
(2)根据溶解度(S)∽温度(T)曲线,操作B的最佳方法为?(填
字母序号)
A.蒸发浓缩,趁热过滤? B.蒸发浓缩,降温结晶,过滤
(3)酸化后Cr2O72-可被SO32-还原成Cr3+,离子方程式为:
?;酸C为?,Cr(OH)3的溶度积常数Ksp[Cr(OH)3]=?。
(4)根据2CrO42-+2H+  ?Cr2O72-+H2O设计图示装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图中右侧电极连接电源的?极,其电极反应式为?。
?Cr2O72-+H2O设计图示装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图中右侧电极连接电源的?极,其电极反应式为?。

参考答案:(1)促进Fe3+水解生成Fe(OH)3而除去;Fe(OH)3
(2)A
(3)3SO32-+Cr2O72-+8H+=2Cr3++3SO42-+4H2O;H2SO4;1.0×10-32mol/L
(4)正极 ,4OH--4e-=O2+2H2O
本题解析:(1)盐类的水解反应是吸热反应,所以微热能促进Fe3+水解生成Fe(OH)3而除去,A为Fe(OH)3;
(2)根据溶解度曲线,可以看出温度较高时,随着温度的升高,Na2SO4的逐渐减少,所以采用蒸发浓缩,趋热过滤的方法,所以A正确;
(3)酸化后,3SO32-+Cr2O72-+8H+=2Cr3++3SO42-+4H2O;因为最终产品是Na2SO4,为避免产生杂质,酸C为?酸;恰好完全沉淀时离子深度为c ≤1.0×10-5mol・L-1,Cr3+完全沉淀时pH=5,c(OH-)=1.0×10-9mol・L-1,所以Cr(OH)3的浓度积常数为Ksp=1.0×10-5×1.0×10-9)3=1.0×10-32
(4)根据示意图知,图中右侧Na2CrO4转化为Na2Cr2O7,需要H+,说明右侧电极发生OH-放电,使H2O的电离平衡向右移动,H+增多,所以右侧电极是连接电源的正极,电极方程式为4OH--4e-=O2+2H2O
本题难度:一般
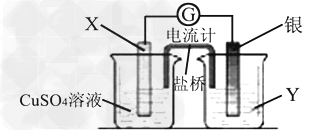
2、选择题 已知反应Cu(s)?+?2Ag+(aq)?=?Cu2+(aq)?+?2Ag(s)为一自发进行的氧化还原反应,将其设计成如图所示原电池。下列说法中正确的是?
[? ]
A.电极X是正极,其电极反应为Cu-2e-?=?Cu2+
B.银电极质量逐渐减小,Y溶液中c(Ag+)增大
C.实验过程中取出盐桥,原电池仍继续工作
D.当X电极质量减少0.64?g时,外电路中有0.02?mol电子转移
参考答案:D
本题解析:
本题难度:一般
3、选择题 下列图示与对应的叙述不相符的是
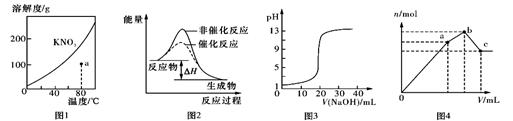
A.图1表示KNO3的溶解度曲线,a点所示的溶液是80℃时KNO3不饱和溶液
B.图2表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化
C.图3表示0.1000mol/LNaOH滴定20.00 mL 0.1000mol/L醋酸的滴定曲线
D.图4表示向NH4Al(SO4)2溶液中逐滴滴入Ba(OH)2溶液,体积V与沉淀n的变化
参考答案:C
本题解析:A正确,a点位于溶解度曲线的下方,是不饱和溶液;B正确,催化剂能改变活化能,但不能改变反应热;C不正确,因为醋酸是弱酸,部分电离,存在电离平衡。所以0.1000mol/L醋酸的pH大于1,而不是等于1;应用氢氧化铝是两性氢氧化物,所以当沉淀达到最大值时,再加入氢氧化钡,沉淀会溶解,D正确,答案选C。
点评:该题容易错选D。这是由于该反应比较复杂,而选项C中的图像变化趋势又是正确的,所以错误的认为C正确,D不正确。因此把握反应的原理,既要分析曲线的变化趋势,更要注意曲线的起点和终点,只有这样才能得出正确的结论。
本题难度:一般
4、选择题 某课外活动小组,为研究金属的腐蚀与防护的原理,做了如下实验:将剪下的一块镀锌铁片,放入锥形瓶中,并滴入少量食盐水将其浸湿,再加数滴酚酞试液,按如图的装置进行实验,过一段时间后观察。下列现象不可能出现的是
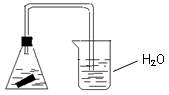
A. B中导气管中产生气泡
B. B中导气管里形成一段水柱
C.金属片剪口变红
D.锌被腐蚀
参考答案:A
本题解析:略
本题难度:简单
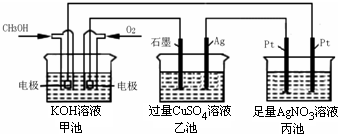
5、选择题 如图所示,下列说法正确的是( )
A.甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置
B.甲池通入CH3OH的电极反应为CH3OH-6e-+2H2O=CO32-+8H+
C.反应一段时间后,向乙池中加入一定量Cu(OH)2固体,能使溶液恢复到原浓度
D.甲池中消耗224mL(标准状况下)O2,此时丙池中理论上最多产生4.32g固体