1、计算题 铁与HNO3作用时,还原产物除与HNO3浓度有关外,还与温度有关。已知在与冷稀HNO3反应时,</PGN0076B.TXT/PGN>主要还原产物为NO气体;在与热的稀HNO3作用时,主要还原产物为N2O气体;当HNO3更稀时,其重要还原产物是NH4+。现有铁与稀HNO3的作用,请分析图10-3,回答有关问题。
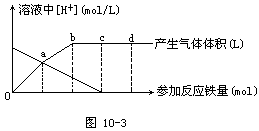
假设曲线的各段内只有一种还原产物。
(1)0点到a点的还原产物是______;
(2)a点到b点的还原产物是______,其原因是______;
(3)试完成b点到c点的反应方程式:
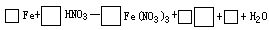
(4)反应过程中,到达______点时HNO3已完全反应。
(5)已知达到d点时,反应结束,此时溶液中的主要阳离子是______;
(6)c点和d点参加反应的铁的物质的量之比是______;
参考答案:(1)NO;(2)N2O,反应放热,使溶液温度升高;(3)8,30,8,3NH4NO3,9;(4)C;(5)Fe2+;(6)2∶3
本题解析:根据图形,应先对气体体积曲线和溶液中[H+]变化曲线作出正确判断。溶液中的[H+]逐渐减小,至c点为0,说明HNO3逐渐参与反应,到c点时恰好反应完全,即0点到c点是铁与HNO3的反应,c点到d点是生成的Fe(NO3)3与铁的反应,到d点时,溶液中生成的Fe(NO3)3完全反应,全部转化为Fe(NO3)2;搞清了[H+]浓度的变化曲线,也就不难理解气体曲线了,只要抓住题目中的已知和铁用量、转移电子数、产生NO或N2O体积的多少的关系及曲线斜率,就不难断定其主要还原产物了。oa:NO,ab:N2O;bc:NH4NO3;cd;Fe(NO3)2。计算c、d点参加反应的铁的物质的量之比时,要明确是0到c铁与HNO3反应生成的Fe(NO3)3,由2Fe(NO3)3+Fe=3Fe(NO3)2可知:生成的Fe(NO3)3的物质的量是cd段“Fe”物质的量的2倍,所以oc段参加反应的铁量是cd段的2倍,这也是本题的巧点。
本题难度:一般
2、填空题 (6分)如图所示,试管中集满干燥的氯气,胶头滴管中装有供反应的足量浓氨水.滴入浓氨水,开始时试管内发生的反应有氧化还原反应:NH3+Cl2→N2+HCl并产生红光和白烟。

请根据以上反应和现象回答下列问题:?
(1)标志反应全部完成的现象是______.
(2)反应完毕后,将试管浸入水中并倒立着试管,取下滴管,有水进入试管,在室温时,进入试管内的水约占试管容积的______。
(3)反应中生成的白烟是______。
(4)用写出试管中反应的化学方程式________。
参考答案:(1)不再产生红光和白烟(2)2/3(3)NH4Cl(4)8NH3+3Cl2=6NH4Cl+N2?
本题解析:由题意知因发生反应8NH3+3Cl2=6NH4Cl+N2时放出大量的热而产生红光和白烟.当不再产生红光和白烟时表明不再放出大量的热,此时反应已经完成.由反应方程式可知,反应产生的N2为参加反应的Cl2的物质的量的(1/3),故进入试管的水的体积约为试管容积的(2/3).显然白烟为NH4Cl。
本题难度:简单
3、计算题 取5.64gCu(NO3)2无水晶体,强热使其分解,得到NO2、O2和2.32固体氧化物。将气体用水充分吸收后,还有气体剩余,同时得到100mL溶液。请通过计算确定:(写出计算过程)
(1)所得溶液的物质的量浓度;
(2)残留固体的成分和质量分别是多少克?
参考答案:(1)0.6mol/L
(2)Cu2O为0.72g(2分),CuO为1.60g
本题解析:假设固体氧化物全部为CuO,则:2Cu(NO3)2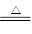 2CuO+4NO2↑+O2↑
2CuO+4NO2↑+O2↑
另外气体被水吸收的方程式为:4NO2+O2+2H2O=4HNO3
可看出,气体将被水全部吸收,且5.64gCu(NO3)2无水晶体( )生成的CuO为0.03×80=2.4g,故固体氧化物中除CuO外,还有Cu2O:4CuO
)生成的CuO为0.03×80=2.4g,故固体氧化物中除CuO外,还有Cu2O:4CuO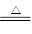 2Cu2O+O2↑
2Cu2O+O2↑
(1)从以上分析可看出,剩余气体为氧气,故N元素全部转化为硝酸,所得溶液的浓度为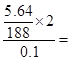 0.6mol/L
0.6mol/L
(2)设固体氧化物中CuO、Cu2O的物质的量分别为x、y
则80x+144y=2.32
再由铜的守恒可知:x+2y=0.03
得:x=0.02mol? y=0.005mol
故CuO、Cu2O的质量分别为1.60g、0.72g
本题难度:简单
4、选择题 下列关于氨气的说法正确的是( )
A.氨气可以用浓硫酸干燥也可用碱石灰干燥
B.氨水能导电,所以NH3是电解质
C.稳定性:NH3<CH4
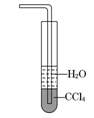
D.用水吸收NH3用右图装置可防止倒吸
参考答案:D
本题解析:氨气是碱性气体,不能用浓硫酸干燥,A不正确。氨水导电,是氨气和水反应生成的一水合氨电离出的离子导致,所以一水合氨是电解质,氨气属于非电解质,B不正确。氮元素的非金属性强于碳元素的,所以氨气的稳定性强于甲烷的,C不正确。因此正确的答案是D。
本题难度:简单
5、选择题 下列叙述不正确的是:
A.五氧化二磷只是磷酸的酸酐
B.二氧化氮不是硝酸的酸酐
C.安全火柴盒的侧面所涂的物质是一种混合物,其中含有红磷和三硫化二锑等
D.含磷的废水拍到自然水中,能引起藻类增殖,使水变质,必须除去
参考答案:A
本题解析:略
本题难度:简单