1、选择题 下列元素不属于主族元素的是( )
A.磷
B.钙
C.锌
D.硅
参考答案:A.P为第ⅤA族元素,属于主族元素,故不选;
B.Ca位于周期表第ⅡA族,属于主族元素,故B不选;
C.Zn位于周期表ⅡB族,不属于主族元素,故C选;
D.Si位于周期表第ⅣA族,属于主族元素,故D不选.
故选C.
本题解析:
本题难度:简单
2、推断题 A、B、C是中学化学中常见的三种短周期元素。已知:
①A元素原子最外层电子数是次外层电子数的2倍;
②B元素最高正价与最低负价的代数和为2;
③C元素有多种化合价,且常温下C元素的单质与某种一元强碱溶液反应,可得到两种含C元素的化合物;
④B、C两种元素质子数之和是A元素质子数的4倍。
(1)写出A元素在周期表中的位置_______________________。
(2)写出C的单质和强碱溶液反应的离子方程式________________________________。
(3)意大利罗马大学的FuNvio?Cacace等人获得了极具理论研究意义的B4气态分子。C4分子结构与白磷分子结构相似 ,已知断裂1?mol?B―B吸收167?kJ的热量,生成1?mol?B≡B放出942?kJ热量。试写出由C4气态分子变成C2气态分子的热化学方程式:____________________________。
,已知断裂1?mol?B―B吸收167?kJ的热量,生成1?mol?B≡B放出942?kJ热量。试写出由C4气态分子变成C2气态分子的热化学方程式:____________________________。
(4)由B、C两种元素组成的化合物X,常温下为易挥发的淡黄色液体,X分子为三角锥形分子,且分子里B、C两种原子最外层均达到8个电子的稳定结构。X遇水蒸气可形成一种常见的漂白性物质。则X的结构式为____________,X与水反应的化学方程式是___________________。
(5)A、B两种元素可形成一种硬度比金刚石还大的化合物Y。在化合物Y中,A、B原子间以单键相结合,且每个原子的最外层均达到8个电子的稳定结构。则Y的化学式为______________,Y晶体的熔点比金刚石熔点______(填“高”或“低”)。
(6)B2H4是一种可燃性液体,其水溶液呈弱碱性,是因为溶液中存在平衡:H2B-BH2+H2O _________________________。
_________________________。
参考答案:
(1)第二周期ⅣA族
(2)Cl2+2OH-=ClO-+H2O
(3)N4(g) ====2N2(g);△H=-882 kJ/mol
(4) ;NCl3+3H2O==== NH3+3HClO?
;NCl3+3H2O==== NH3+3HClO?
(5)C3N4;高
(6)H2B-BH3++OH-(或B2H5++OH-)
本题解析:
本题难度:一般
3、推断题 有A、B、C、D、E五种元素,其中A、B、C属于同一周期,A原子最外层p能级的电子数等于次外层的电子总数,C原子最外层中有2个不成对的电子。已知C、D、E原子核内的质子数均与中子数相等,且C元素可分别与A、B、D、E生成RC2型化合物,在DC2中,D与C的质量比为7:8,在EC2中,E与C的质量比为1:1。请回答下列问题:
(1)写出A、E两种元素的元素符号:A____、E____。
(2)写出D原子的电子排布式____________。
(3)指出E在元素周期表中的位置____________。
(4)比较A、B、C三种元素的第一电离能的大小顺序____________。
(5)比较D和E元素的电负性的相对大小____________。
参考答案:(1)C;S
(2)1s22s22p63s23p2
(3)第三周期,第ⅥA族
(4)C<O<N
(5)Si<S
本题解析:
本题难度:一般
4、填空题 下图是元素周期表的短周期部分,序号a~h代表8种常见元素.
| IA | | O族
第一周期
a
IIA | IIIA
IVA
VA | VIA
VIIA
第二周期
|
b
c | d
第三周期
e
| f
| g
h
|
请用相应的化学用语回答下列问题:
(1)画出g原子结构示意图______.
(2)写出元素h的单质与元素a、c形成的简单化合物发生置换反应的化学方程式______.
(3)写出f单质与a、d、e三种元素形成的化合物水溶液反应的化学方程式______.
(4)a、b元素形成的最简单化合物与d单质可组成燃料电池(以KOH溶液作电解质溶液),写出正极的电极反应式:______,负极发生______反应(填“氧化”或“还原”),OH-移向______极.
参考答案:根据元素在周期表中的分布知识,可以推知a是H,b是C,c是N,d是O,e是Na,f是Al,g是S,h是Cl.
(1)S原子结构示意图为:
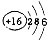
,故答案为:
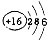
;
(2)元素a、c形成的简单化合物是氨气,元素h的单质是氯气,氯气和氨气的反应为:3Cl2+2NH3=N2+6HCl,故答案为:3Cl2+2NH3=N2+6HCl;
(3)f单质是金属铝与a、d、e三种元素形成的化合物水溶液氢氧化钠反应的化学方程式为:2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑,故答案为:2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑;
(4)a、b元素形成的最简单化合物是甲烷,和氧气形成的甲烷燃料电池中,正极上放电的是氧气,发生得电子得还原反应,电极反应是O2+2H20+4e-=4OH-,负极上是燃料甲烷失电子,发生氧化反应,在原电池中,阴离子移向原电池的负极,故答案为:O2+2H20+4e-=4OH-;氧化;负.
本题解析:
本题难度:一般
5、选择题 某一周期ⅡA族元素的原子序数为x,则同周期的ⅢA族元素的原子序数( )
A.只有x+1
B.可能是x+8
C.可能是x+2
D.可能是x+1或x+11或x+25
参考答案:因为是同一周期的IIA族,即同一横行往右一个主族,在第二、三周期原子序数增加一,因而可以x+1;
又因为IIA族与IIIA族元素在第四周期起有过渡元素,因而又可以x+11;
在第六、七周期的过渡元素中又出现镧系和锕系,因而又可以x+25.
故选D.
本题解析:
本题难度:简单