1、选择题 电池是人类生产和生活中重要的能量来源。各式各样电池的发明是化学对人类的一项重大贡献。下列有关电池的叙述正确的是
[? ]
A.锌锰干电池工作一段时间后碳棒变细
B.氢氧燃料电池可将热能直接转变为电能
C.氢氧燃料电池工作时氢气在负极被氧化
D.太阳能电池的主要材料是高纯度的二氧化硅
参考答案:C
本题解析:
本题难度:一般
2、选择题 在无土栽培中,需配制一定量含50 mol NH4Cl、16 mol KCl 和24 mol K2SO4的营养液。若用KCl、NH4Cl和(NH4)2SO4三种固体为原料来配制,三者物质的量依次是(单位
为mol)?(?)
A.2、64、24
B.64、2、24
C.32、50、12
D.16、50、24
参考答案:B
本题解析:50 mol NH4Cl、16 mol KCl 和24 mol K2SO4的营养液中,NH4+的总物质的量为50 mol、K+的总物质的量为16+24×2=64mol、CL-的总物质的量为50+16=66mol、SO42-的总物质的量为24mol,根据质量守恒定律可得:KCl、NH4Cl和(NH4)2SO4三种固体物质的量依次是64、2、24mol;正确选项为B;
本题难度:简单
3、选择题 银锌碱性电池的电解质溶液为浓KOH溶液,放电时的总反应为:
Ag2O2+2Zn+4KOH+2H2O=2K2Zn( OH )4+2Ag下列有关该电池的说法不正确的是
A.电池放电时,正极附近溶液的碱性增强
B.电池放电时,负极反应为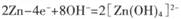
C.电池充电时,阳极反应为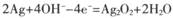
D.充电时锌极与外电源正极相连
参考答案:D
本题解析:原电池中负极失去电子,发生氧化反应,正极得到电子,发生还原反应,所以根据放电的总方程式可知,正极和负极的电极反应式分别是Ag2O2+4e-+2H2O=2Ag+4OH-、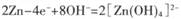 ,所以选项AB都是正确的。充电相当于是放电的逆反应,所以选项C正确,D不正确,锌极应该与外电源的负极选项,答案选D。
,所以选项AB都是正确的。充电相当于是放电的逆反应,所以选项C正确,D不正确,锌极应该与外电源的负极选项,答案选D。
本题难度:简单
4、选择题 我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应
产生电流。电池总反应为:4A1+3O2+6H2O=4A1(OH)3,下列说法不正确的是( )
A.正极反应式为:O2+2H2O+4e--=4OH--
B.电池工作时,电流由铝电极沿导线流向铂电极
C.以网状的铂为正极,可增大与氧气的接触面积
D.该电池通常只需更换铝板就可继续使用