1、选择题 同温同压下,下列各热化学方程式中反应热数值最小的是( )
A.2A(l)+B(l)=2C(g);△H=+Q1kJ?mol-1
B.2A(g)+B(g)=2C(g);△H=+Q2kJ?mol-1
C.2A(g)+B(g)=2C(l);△H=+Q3kJ?mol-1
D.2A(l)+B(l)=2C(l);△H=+Q4kJ?mol-1
参考答案:C
本题解析:
本题难度:简单
2、选择题 氢气(H2)、一氧化碳(CO)、辛烷(C8H18)、甲烷(CH4)的热化学方程式分别为:
H2(g) + 1/2O2(g) = H2O(l);△H= -285.8 kJ/mol
CO(g) + 1/2O2(g) = CO2(g);△H= -283.0 kJ/mol
C8H18(l) + 25/2O2(g) = 8CO2(g) + 9H2O(l);△H= -5518 kJ/mol
CH4(g) + 2O2(g) = CO2(g) + 2H2O(l);△H= -890.3 kJ/mol
相同质量的H2、CO、C8H18、CH4完全燃烧时,放出热量最少的是
[? ]
A.H2(g)
B.C8H18(l)
C.CO(g)
D.CH4(g)
参考答案:C
本题解析:
本题难度:一般
3、填空题 火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当把0.4mol液态肼和0.8molH2O2混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃.101 kPa下测得的热量)。
(1)反应的热化学方程式为_______________________。
(2)又已知H2O(l)=H2O(g) ΔH=+44kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是_____________kJ。
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是__________________________。
参考答案:(1)N2H4(l)+2H2O2(l)==N2(g)+4H2O(g) △H=-644.25 KJ/mol
(2)410.125
(3)产物不会造成环境污染
本题解析:
本题难度:一般
4、填空题 2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示。
2SO3(g)反应过程的能量变化如图所示。
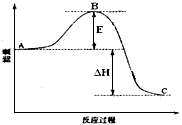
已知1mol SO2(g)氧化为1mol SO3的ΔH=-99kJ・mol-1.请回答下列问题:
(1)图中A、C分别表示_______、_________ ,E的大小对该反应的反应热有无影响?______ 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是低?________ ,理由是________________ ;
(2)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式:_____________________________________;
(3)图中△H _____________-kJ・mol-1;
(4)已知单质硫的燃烧热为296 KJ・mol-1,计算由S(s)生成3 molSO3(g)的 △H= ______kJ・mol-1。?
参考答案:(1)反物能量;生成物能量; 无; 降低; 因为催化剂改变了反应的历程使活化能E降低
(2)SO2 +V2O5=SO3+2VO2 ? 4VO2+ O2=2V2O5?
(3)-198?
(4)-1185
本题解析:
本题难度:一般
5、选择题 100gC不完全燃烧所得产物中,CO所占体积为1/3,CO2为2/3,且
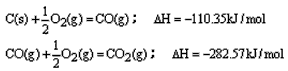
与这些碳完全燃烧相比,损失的热量为
[? ]
A.39.292kJ
B.3274.3kJ
C.784.92kJ
D.2489.44kJ
参考答案:C
本题解析:
本题难度:一般