1���ƶ��� ��ͼ��һЩ�����ĵ��ʺͻ�����֮���ת����ϵͼ����Щ��Ӧ�еIJ������ʱ���ȥ�����³�ѹ�£�AΪ��ɫ�ж����壬BΪ����ɫ��ĩ��C��EΪ��������õĽ������ʣ�JΪ���ɫ���壬LΪ�������������Ӧ�١��ھ�Ϊ��ҵ�ϵ���Ҫ��Ӧ��
��ش��������⣺?
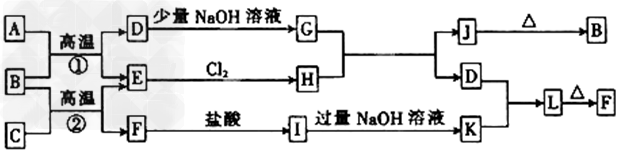
(1)д��B�Ļ�ѧʽΪ_________��D�ĵ���ʽΪ______________��?
(2)��ɵ���C��Ԫ����Ԫ�����ڱ��е�λ��Ϊ_________________��
(3)д����I��Һ�м������NaOH��Һʱ������Ӧ�����ӷ���ʽ____________________��
(4)д����Na2SiO3��Һ��ͨ������Dʱ������Ӧ�����ӷ���ʽ___________________��
�ο��𰸣�(1)Fe2O3��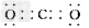
(2)��������IIIA��
(3)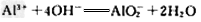
(4)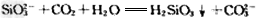
���������
�����Ѷȣ�һ��
2������� ��6�֣���֪����A��B��C��D��E��F��G��H��I��J��X��Y������ͼ��ʾ��ת����ϵ����������A��B��CΪ�����ǽ������ʣ�X��YΪ�����������ʡ�(���ַ�Ӧ��������û��ȫ���г�����Ӧ����δȫ���г�)

�밴Ҫ��ش��������⣺
��1������E�ĵ���ʽΪ?��
��2��G�Ļ�ѧʽ��___________��
��3��д����Ӧ��I��J�������ӷ���ʽ?��
��4������X��NaOH��Һ��ӦҲ�ܵõ���ҺH����д����Ӧ�Ļ�ѧ����ʽ?��
�ο��𰸣���6�֣���1��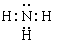 ��2��Al(OH)3
��2��Al(OH)3
��3��2Fe2����Cl2��2Fe3����2Cl��?��4��2Al+2NaOH+2H2O��2NaAlO2+3H2��
�����������ҺD�ܺͶ��������ڼ��ȵ��������������壬��˵��DӦ����Ũ���ᣬC������������Y�ܺ����ᷴӦ������ҺI����I�ܺ�����������Ӧ����˵��YӦ���DZ�۵Ľ�������Y��������I���Ȼ�������J���Ȼ�����B��������Ӧ�����Ȼ��⣬����B����������ɫ����G����������������Һ�У�˵��G��������������X��Al��F���Ȼ�����F�ܺ�E��Ӧ����������������E�����壬����E�ǰ�������A�ǵ�����
�������������е��Ѷȵ����⣬�����ۺ���ǿ�����������������ͽ��ⷽ����ѵ��������������ѧ���������������ʹ���˼ά�������������Ҫѧ����ȷ���ǻ�ѧ�ƶ�����һ���ۺ��Խ�ǿ�����⣬��Ԫ�ؼ����������ʺ�������������������ѧ�����֪ʶ����������ѧ�Ƽ��ۺϡ��������ɿ���ѧ���Ի�ѧ֪ʶ������̶ȣ�����Ҫ��������ѧ�����ۺϷ���������˼ά���������ͼ��ķ�������ؼ�����Ѱ�ҡ�ͻ�ƿڡ�����ͻ�ƿڡ�����ץ���ء��֣�����������ɫ������״̬��������ζ�����ⷴӦ���������������Ʒ���������;�ȡ�
�����Ѷȣ�����
3��ѡ���� ���мס��ҡ�����������5�����ʣ���һ�������£������ܰ���ͼ��ʽ����ת����
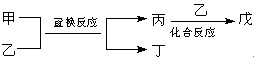
���ƶ���ȷ����
ѡ��
| ��
| ��
| ��
| ��
| ��
|
A
| NH3
| O2
| NO
| H2O
| NO2
|
B
| Mg
| CO2
| C
| MgO
| CO
|
C
| C
| H2O
| CO
| H2
| HCOOH
|
D
| FeBr2
| Cl2
| FeCl2
| Br2
| FeCl3
|
?
�ο��𰸣�B
���������A������û���Ӧ���ͣ�����B����ȷ��C����CO���������ܻ��������죬����D�����������û���Ӧ�����ɱ�Ӧ�������������ӣ�����ѡ��B��
�����Ѷȣ���
4������� ��֪A��BΪ�����Ľ������ʣ�C��DΪ�����ķǽ������ʣ��ס��ҡ���Ϊ���ֳ����Ļ����������ѧ��ѧ�г����ĺ���ɫ��ĩ״���壬����֮����ת����ϵ��ͼ��ʾ(���ֲ��P��Ӧ����û���г�)��
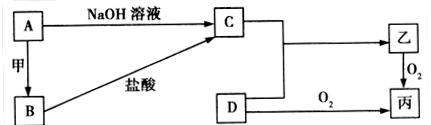
(1)д����ͼ��Aת��ΪB�Ļ�ѧ����ʽ��_______________________________________���÷�Ӧ����______________(����ȷ�Ӧ�����ȷ�Ӧ��)��
(2)���ҵ�ˮ��Һ�������ԣ�����һ�ִ�����Ⱦ��д̼�����ζ����֪16 g���嵥��D��ȫȼ��ת���ɱ�ʱ���ų�148.4 kJ����������÷�Ӧ���Ȼ�ѧ����ʽΪ��
_____________________________________________________________________________��
(3)������ˮ��Һ�г������ԣ����ο��������ʣ���C��D���������ҵķ�Ӧ�ǿ��淴Ӧ��
�ٽ������ʵ�����C��D���ֵ��ʳ���һ����㶨���ܱ������У����ʵ������ͺ��������·�Ӧ������˵���в���ȷ����____________(����ĸ)��
a.�ﵽ��ѧƽ��ʱ��2����(C) = 3����(��)
b.��Ӧ�����У�D���ʵ��������ʼ��Ϊ50%
c.�ﵽ��ѧƽ��ʱ�����������ܶȱ��ֲ���
d.�ﵽ��ѧƽ��Ĺ����У������ƽ����Է�������������
e.�ﵽ��ѧƽ����������¶ȣ��ҵ������������
������һ�����Ϊ10 L���ܱ������У�����8 mol C���ʺ�2 mol D���ʣ���һ���¶��·�����Ӧ���������ң���40 min��Ӧ�ﵽƽ�⣬��ʱC��ת����Ϊ37.5%���ӷ�Ӧ��ʼ����ƽ���40 min�ڣ��������ұ�ʾ�Ļ�ѧ��Ӧ����Ϊ_________________________���ﵽƽ������������а�5��1��2�����ʵ���֮���ٴγ���C��D�����������ʣ���ԭƽ����ϵ��C��ת���ʽ�_____________(���������С�����䡱)��
�ο��𰸣�(1)2Al + Fe2O3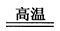 ? Al2O3 + 2Fe(2��)?���ȷ�Ӧ(1��)
? Al2O3 + 2Fe(2��)?���ȷ�Ӧ(1��)
(2)S(s) + O2(g) = SO2(g)����H ="�C296.8" kJ/mol (2��)
(3)��e (2��)? ��0.005 mol/(L?min) (2��)?���� (1��)
�����������
�����Ѷȣ���
5������� ����ɫ���嵥�ʼ����պ�Ͷ��D��Ũ��Һ�У����߾��ҷ�Ӧ������̬�����A��������������ͼ��ʾ����һϵ��ת����
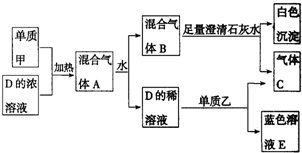
��ش��������⣺
��1������C��______����ҺE��������______���û�ѧʽ��ʾ����
��2��д�����ʼ���D��Ũ��Һ��Ӧ�Ļ�ѧ����ʽ______��
��3��д������Bͨ����������ʯ��ˮ�з�����Ӧ�����ӷ���ʽ______��
�ο��𰸣�D��ϡ��Һ�뵥���ҷ�Ӧ���Եõ���ɫ��ҺE����E��Һ����ͭ���ӣ����ת����ϵ��֪����ΪCu��DΪ���ᣬ��EΪCu��NO3��2����Ӧ���ɵ�CΪNO��
��ɫ���嵥�ʼ���Ũ���ᷴӦ�õ��������A��A����ˮ�õ�ϡ������������B��B��������ʯ��ˮ��Ӧ�õ���ɫ������NO�����ɫ����ΪCaCO3��BΪCO2��NO������壬AΪCO2��NO2������壬�ʼ�Ϊ̼���ʣ�
��1��������������֪������C��NO����ҺE��������Cu��NO3��2��
�ʴ�Ϊ��NO��Cu��NO3��2��
��2������̼��Ũ���ᷴӦ�Ļ�ѧ����ʽΪ��C+4HNO3��Ũ����.CO2��+4NO2��+2H2O��
�ʴ�Ϊ��C+4HNO3��Ũ����.CO2��+4NO2��+2H2O��
��3������Bͨ����������ʯ��ˮ�з�����Ӧ�����ӷ���ʽΪ��Ca2++CO2+2OH-�TCaCO3��+H2O��
�ʴ�Ϊ��Ca2++CO2+2OH-�TCaCO3��+H2O��
���������
�����Ѷȣ�һ��