1、实验题 甲、乙两人分别用不同的方法配制100ml 3.0mol/L的H2SO4溶液。
(1)甲:量取25.0 ml 12 mol/L浓H2SO4倒入加入约25mL 蒸馏水的烧杯中,搅拌均匀,待冷却至室温后转移到100 ml 容量瓶中,用少量的水将烧杯等仪器洗涤2~3次,每次洗涤液也转移到容量瓶中,然后小心地向容量瓶加入水至刻度线定容,塞好瓶塞,反复上下颠倒摇匀。 实验所用的玻璃仪器除烧杯和胶头滴管外,还有的玻璃仪器有?,?,?;
蒸馏水的烧杯中,搅拌均匀,待冷却至室温后转移到100 ml 容量瓶中,用少量的水将烧杯等仪器洗涤2~3次,每次洗涤液也转移到容量瓶中,然后小心地向容量瓶加入水至刻度线定容,塞好瓶塞,反复上下颠倒摇匀。 实验所用的玻璃仪器除烧杯和胶头滴管外,还有的玻璃仪器有?,?,?;
(2)乙:用100 ml 量筒量取25.0 ml 12 mol/L浓H2SO4,并向其中小心地加入少量水,搅拌均匀,待冷却至室温后,再加入水至100 ml 刻度线,再搅拌均匀。
你认为此法是否正确??。若不正确,指出其中错误 之处?,?。
之处?,?。
参考答案:
本题解析:略
本题难度:简单
2、实验题 (14分)单晶硅是信息产业中重要的基础材料。通常用碳在高温下还原二氧化硅制得粗硅(含铁、铝、硫、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450-500°C),四氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。查阅相关资料获悉: a.四氯化硅遇水极易水解;
b.铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
c.有关物质的物理常数见下表:
物质
| SiCl4
| AlCl3
| FeCl3
| PCl5
|
沸点/℃
| 57.7
| ―
| 315
| ―
|
熔点/℃
| -70.0
| ―
| ―
| ―
|
升华温度/℃
| ―
| 180
| 300
| 162
|
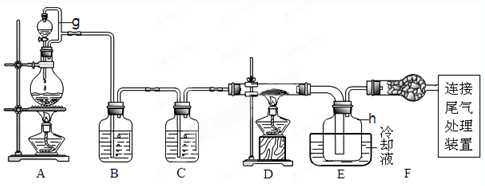
请回答下列问题:
(1)写出装置A中发生反应的离子方程式?。
(2)装置A中g管的作用是?;装置C中的试剂是?;装置E中的h瓶需要冷却理由是?。
(3)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中,含有铁、铝等元素的杂质。为了分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原反应滴定,锰元素被还原为Mn2+。
①写出用KMnO4滴定Fe2+的离子方程式:?;
②滴定前是否要滴加指示剂??(填“是”或“否”),判断滴定终点的方法是?。
③某同学称取5.000g残留物,预处理后在容量瓶中配制成100ml溶液,移取25.00ml试样溶液,用1.000×10-2mol・ L-1KMnO4标准溶液滴定。达到滴定终点时,消耗标准溶液20.00ml,则残留物中铁元素的质量分数是?。若滴定前平视,滴定后俯视KMnO4液面,对测定结果有何影响?(填“偏高”、“偏低”、或“无影响”)
参考答案:(1)MnO2+4H++2Cl- Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
(2)平衡压强,使液体顺利滴下;浓硫酸;使SiCl4冷凝
(3)①5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
②否(1分);当滴入最后一滴KMnO4溶液时,溶液颜色由无色变为紫色,且30秒不褪色;(2分)③4.480% ;偏低(各2分)
本题解析:(1)装置A是制取氯气的,所以发生反应的离子方程式是
MnO2+4H++2Cl- Mn2++Cl2↑+2H2O。
Mn2++Cl2↑+2H2O。
(2)要使分液漏斗中的液体顺利滴下,所以作用是平衡压强,使液体顺利滴下;应用四氯化硅遇水极易水解,所以在通入装置D之前需要,需要干燥处理,即装置C中的试剂是浓硫酸;SiCl4的熔点较低,所以作用是使SiCl4冷凝。
(3)①酸性高锰酸钾溶液就有强氧化性,能把亚铁离子氧化生成铁离子,反应的方程式是5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O。
②由于酸性高锰酸钾溶液,在溶液中显紫红色,所以不需要另加指示剂。因此终点时的现象是当滴入最后一滴KMnO4溶液时,溶液颜色由无色变为紫色,且30秒不褪色。
③根据反应式可知,25.00ml溶液中亚铁离子的物质的量是0.0200L×0.01mol/L×5=0.001mol,所以残留物中铁元素的质量分数是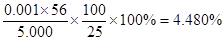 ;若滴定前平视,滴定后俯视KMnO4液面,则消耗高锰酸钾溶液的体积减少,则测定结果偏低。
;若滴定前平视,滴定后俯视KMnO4液面,则消耗高锰酸钾溶液的体积减少,则测定结果偏低。
本题难度:一般
3、选择题 用下列实验装置完成对应实验(部分仪器已省略),不能达到实验目的是( )
A.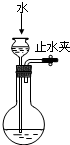
检查装置气密性
B.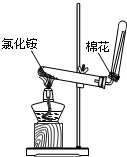
实验室制氨气
C.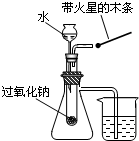
验证过氧化钠与水反应既生成氧气又放热
D.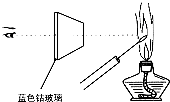
检验K2CO3中的K+
参考答案:A.用弹簧夹夹住右边导管,向长颈漏斗中倒水,液面高度不变,说明装置气密性良好,故A正确;
B.实验室用氯化铵和碱石灰反应制取氨气,即碱与盐反应生成新碱和新盐,化学方程式为:2NH4Cl+Ca(OH)2△.CaCl2+2NH3↑+2H2O,氯化铵分解生成氨气和氯化氢,氨气和氯化氢冷却生成氯化铵,无法制取纯净的氨气,故B错误;
C.2H2O+2Na2O2=O2↑+4NaOH,把一根带火星的木条放在管口处,木条复燃,证明是氧气,盛放过氧化钠的试管是封闭的,封闭了一段空气,当过氧化钠和水反应放热,气体被加热,体积膨胀,通过支管向烧杯中排放,看到烧杯水中有气泡说明该反应放热,故C正确;
D.在进行焰色反应时,由于Na+燃烧呈黄色,干扰了K+的焰色反应(紫色)的观察,所以必须把黄色的光滤去,透过蓝色钴玻璃观察K+的焰色反应(紫色),故D正确;
故选B.
本题解析:
本题难度:一般
4、选择题 下列物质中能用于萃取溴水中溴的是?
A?氢氧化钠溶液? B.裂化汽油? C.酒精? D.苯
参考答案:D
本题解析:略
本题难度:简单
5、选择题 下面哪个图是以乙酸(沸点:118℃)、浓硫酸和乙醇(沸点:78.5℃)为原料合成乙酸乙酯(沸点:77℃)的最佳装置?(?)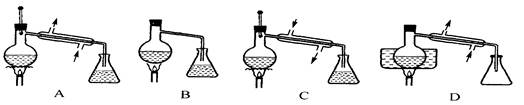
参考答案:A
本题解析:冷凝水应该下进上出!要通过温度计严格控制反应温度,不能太高!采用酒精灯光直接加热。
本题难度:简单