1、选择题 25℃时,某一元酸(HB)的盐NaB的水溶液呈碱性,下列叙述正确的是
[? ]
A.HB的电离方程式为:HB==H++B-
B.NaB溶液中:c(Na+)>c(B-)>c(H+)>c(OH-)
C.NaB溶液中存在如下关系:c(Na+)+c(H+)==c(HB)+c(B-)
D.0.1mol/L NaB溶液中水电离的OH-浓度大于10-7mol/L
参考答案:D
本题解析:
本题难度:一般
2、选择题 下列说法正确的是
[? ]
A. 25℃时,0.1 mol/L pH=4.5的NaHC2O4溶液:c(HC2O4-)>c(H2C2O4)>c(C2O42-)
B. 相同温度下,pH相等的Na2CO3溶液、C6H5ONa(苯酚钠)溶液、NaOH溶液:c(C6H5ONa)>c(Na2CO3)>
c(NaOH)
C. 常温下,将CH3COONa溶液、HCl溶液混合所得中性溶液:c(Na+)>c(Cl-)=c(CH3COOH)
D. 0.1 mol/L Na2CO3溶液与0.1mol/L NaHCO3溶液等体积混合所得溶液:c(CO32-)+2c(OH-)=c(HCO3-)+
c(H2CO3)+2c(H+)
参考答案:BC
本题解析:
本题难度:一般
3、选择题 苏打水是一种新兴的饮料,其有效成份是碳酸氢钠.下列有关说法错误的是( )
A.苏打水要存放在冷暗处
B.苏打水显弱酸性
C.碳酸氢钠可用于治疗胃酸过多
D.小苏打在食品加工中常作疏松剂
参考答案:B
本题解析:
本题难度:一般
4、填空题 某二元酸(化学式用H2A表示)在水中的电离方程式是:H2A H++HA-,HA-
H++HA-,HA-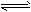 H++A2-,
H++A2-,
回答下列问题:
(1)Na2A溶液呈________(填“酸性”、“中性”或“碱性”),理由是:_______________________
(用离子方程式说明) NaHA溶液呈________(填“酸性”、“中性”或“碱性”),理由是:________________________。
(2)已知0.1mol/LNaHA溶液的pH=2,则0.1mol/L的H2A溶液中氢离子的物质的量浓度________0.11mol/L(填“<”、“>”或“==”)理由是:______________________________。
(3)0.1mol/LNaHA溶液中各种离子浓度由大到小的顺序是:________________________
参考答案:(1)碱性;A2-+H2O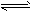 HA-+OH-;酸性;该酸式盐只能电离,导致溶液中c(H+)>c(OH-),溶液呈酸性
HA-+OH-;酸性;该酸式盐只能电离,导致溶液中c(H+)>c(OH-),溶液呈酸性
(2)<;在H2A中HA-电离受到H2A第一步电离产生的H+的影响,对HA-电离有抑制作用,导致HA-电离比NaHA中HA-电离小
(3)c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
本题解析:
本题难度:一般
5、选择题 下列说法正确的是
[? ]
A.常温下0.4 mol/L HB溶液和0.2 mol/L NaOH溶液等体积混合后溶液的pH=3,则混合溶液中离子浓度的大小顺序为:c(Na+)>c(B-)>c(H+)>c(OH-)
B.常温时,pH =2的CH3COOH溶液和HCl溶液、pH=12的氨水和NaOH溶液,四种溶液中由水电离的c(H+)相等
C.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色
D.0.1mol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-)
参考答案:C
本题解析:
本题难度:一般