1、填空题
(1)画出这两种固体分子的几何构型图:_________。
(2)黄绿色固体溶解度大的原因是:_________。
参考答案:
(1)淡黄色溶解度小的是
 ?
?
黄绿色固体溶解度大的是
 ?
?
(2)因为分子结构不对称,所以分子有极性,因而在水中溶解度大。
本题解析:PtCl2(NH3)2可能的平面正方形结构有:
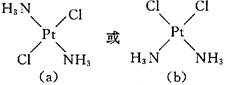 ?
?
a中结构对称,因此分子无极性。由相似相溶原理可知,它在极性分子水中溶解度小,而b的分子有极性,所以水溶性大。
本题难度:一般
2、选择题 下列叙述正确的是?
[? ]
A.金属与盐溶液反应都是置换反应
B.阴离子都只有还原性
C.与强酸、强碱都反应的物质只有两性氧化物或两性氢氧化物
D.分子晶体中都存在范德瓦尔斯力,可能不存在共价键
参考答案:D
本题解析:
本题难度:简单
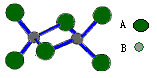
3、选择题 某无机化合物的二聚分子结构如图,该分子中A、B两种元素都是第三周期的元素,分子中所有原子最外层都达到8电子稳定结构。下列关于该化合物的说法不正确的是
[?]
A.化学式是Al2Cl6
B.不存在离子键和非极性共价键
C.在固态时所形成的晶体是分子晶体
D.是离子化合物,在熔融状态下能导电
参考答案:D
本题解析:
本题难度:简单
4、选择题 下列对有关微粒结构的表示或说法不正确的是?(?)
A.氮分子的电子式为::N:::N:
B.氨分子的空间构型为三角锥型,属于极性分子
C.白磷属于分子晶体,空间构型为正四面体,键角60°,是非极性分子
D.NH4+离子中的四个N―H键虽然形成方式不同,但键能、键长、键角都相同
参考答案:A
本题解析:在A中,氮气分子中两个氮原子之间以三键结合,三对共用电子对应该纵向排列,因每个氮原子各提供三个电子。
本题难度:一般
5、选择题 X、Y均为短周期元素,且X位于IA族,Y位于VIA族.下列说法中,正确的是( )
A.同周期中X的原子半径大于Y的原子半径
B.X、Y形成的化合物X2Y溶于水后溶液均呈碱性
C.X、Y形成的离子化合物中只含有离子键
D.1?mol?由X、Y组成的化合物所含有的电子总数均为18×6.02×1023
参考答案:A、同周期原子半径从左向右在减小,则同周期中X的原子半径大于Y的原子半径,故A正确;
B、X、Y形成的化合物X2Y若为H2O显中性,若为H2S显酸性,若为Na2O显碱性,故B错误;
C、X、Y可以形成离子化合物过氧化钠,过氧化钠中含有离子键、非极性键,故C错误;
D、由X、Y组成的化合物有H2O、H2S、H2O2、Na2O、Na2S、Na2O2等,1molH2O中含有10mol电子,1molNa2O含有30mol电子、1molNa2S含有38mol电子、1molNa2O2含有38mol电子,则1mol由X、Y组成的化合物所含有的电子总数还可能为10×6.02×1023或其它,故D错误.
故选A.
本题解析:
本题难度:简单