1��ʵ���� ��10�֣�Ϊ���ڡ����������ʺ���;����ij��ʦ���ö������̺�Ũ����Ϊ��Ҫԭ�ϣ����һ����ͼ��ʾ��ʵ��װ��(����A������ע������ͷ�� ��Ƥ�ܣ���ͷ�Ѳ��벢������Ƥ��)���н�ѧ���Իش��������⣺
��Ƥ�ܣ���ͷ�Ѳ��벢������Ƥ��)���н�ѧ���Իش��������⣺
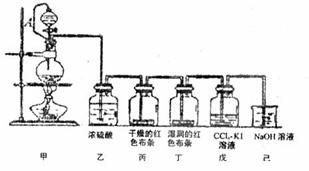
��1��������ƿ������Ӧ�Ļ�ѧ����ʽΪ?��
��2�����������?��
���е����ӷ���ʽ��______________________________����
��3��������Ƥ�ܽ���Һ©���϶�����ƿ��ͨ����������?��
��4����֪��������ˮ��Ӧ�Ļ�ѧ����ΪCl2 + H20 =" HCl" +? HClO��
������Ϊʹ��ɫ������ɫ��������?��
��Ϊ̽�����������Ư����,����Ƽ�ʵ�����֤����д��ʵ��IJ�������������ͽ���
�ο��𰸣���10�֣�(1) 4HCl(Ũ)+Mn02 ==MnCl2+C12��+2H20?��2�֣�

�����������
�����Ѷȣ���
2������� ��18�֣�������ijͬѧ�о��������ʹ����е�һ��Ƭ�ϡ������������ɲ���ʵ�鲢��ȫʵ���¼��
[�۲�]��������ɫ��״̬��?ɫ?״̬������������ζ��?��ζ��
[Ԥ��]������һ�ַǽ������ʣ������ܾ���������?��
��Ԫ�ػ��ϼ۵ĽǶȷ����������ܾ���������?��
[ʵ��̽��]
[ʵ�����]
��1��ͨ���Ƚ�����������ѧϰ���������ȷǽ������ʵ����ʣ�����֪�����Ļ�ѧ��?������?��Ӧ��
��2�������������У���ͬѧ���õ�����Щ�о��������ʵķ�����
?��
��3��˵����������ζ�ķ�����?��
�ο��𰸣�
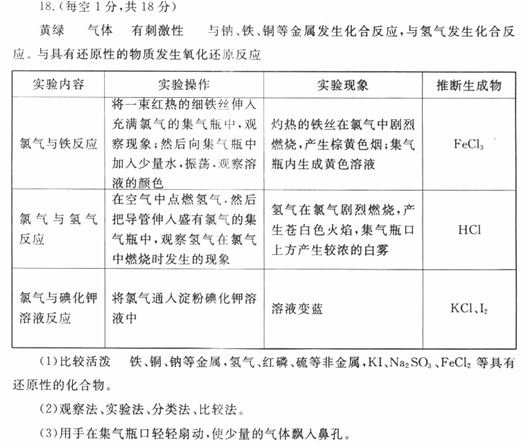
�����������
�����Ѷȣ�һ��
3��ѡ���� ����ˮ�д��ڶ��ַ��Ӻ����ӣ���ͨ��ʵ��ķ�������ȷ��������˵���п��ܴ�����ǣ�������
A�����뺬��NaOH�ķ�̪��Һ����ɫ��ȥ��˵����H+����
B��������ɫ��������ɫ������ɫ��˵����HClO���Ӵ���
C����ˮ��dz��ɫ�����д̼�����ζ��˵����Cl2���Ӵ���
D�����������ữ��AgNO3��Һ������ɫ������˵����Cl-����
�ο��𰸣�����ͨ����Һ�У���ˮ��Ӧ����Cl2+H2O�THCl+HClO����ˮ�д���Cl2��H2O��HClO��H+��Cl-��ClO-��OH-��
A��������̪��죬H+��Ӧʹ��ɫ��ʧ�������������Ư���ԣ�Ҳ��ʹ��ɫ��ȥ������˵����H+���ڣ���A����
B�����������Ư���ԣ��������ɫ��������ɫ������ɫ��˵����HClO���Ӵ��ڣ���B��ȷ��
C������Ϊ����ɫ���壬���д̼�����ζ������ˮ��dz��ɫ�����д̼�����ζ��˵����Cl2���Ӵ��ڣ���C��ȷ��
D����AgCl������ˮ������������ữ��AgNO3��Һ������ɫ������˵����Cl-���ڣ���D��ȷ��
��ѡA��
���������
�����Ѷȣ�һ��
4��ѡ���� ���й���F��Cl��Br��I�ıȽ��У�����ȷ����
A�����ǵ�ԭ�Ӻ�����Ӳ�����ԭ�����������Ӷ�����
B��������±�ص��ʴ�±�������û������Ŀ�������ԭ�����������Ӷ�����
C�����ǵ��⻯����ȶ�����ԭ�����������Ӷ���ǿ
D�����ǵĵ�����ɫ��ԭ�����������Ӷ�����
�ο��𰸣�C
�����������
�����Ѷȣ���
5��ѡ���� ��һ��Ͳ�г���1/4�����Cl2����1/4�����N2����1/2�����H2�������չ�����һ��ʱ�䣬�����������ȫ�����ɫ���������䵹����ʢˮ��ˮ���У�������ͬ�����½�����Ͳ��ˮ�����ռ��Ͳ�ݻ���
A��1/2
B��1/3
C��1/4
D��3/4
�ο��𰸣�A
����������չ������1/4�����Cl2�����1/4�����H2����Ӧ����1/2�����HCl�����ٵ���ˮ�ۣ�1/2�����HCl��������ˮ�У���ʱֻʣ��1/4�����H2����1/4�����N2��������ѡ��A�
������������뷴Ӧ�������Լ���Ӧ�����������͵õ���ȷ�𰸣����ڼ�����
�����Ѷȣ�һ��