|
�߿���ѧ���⡶�й�������ԭ��Ӧ�ļ��㡷��ϰ��(��)
2021-02-18 07:34:42
�� �� �� ��
|
1��ѡ���� 2H2O2=2H2O+O2 2KClO3=2KCl+3O2 2HgO=2Hg+O2 2Na2O2+2CO2=2Na2CO3+O2��
��Ҫ�Ʊ�������O2����ת�Ƶĵ�����֮��Ϊ �� ��
A��1��1��1��1
B��1��2��2��1
C��2��1��1��2
D��1��2��1��2
|
�ο��𰸣�B
�����������
�����Ѷȣ�һ��
2��ѡ���� �йػ�ѧ������ȷ����
��?
A�����Ľṹ��ʽC6H6��������
B����ϩ�Ľṹ��ʽCH2CH2
��
C�����Ȼ�̼�ĵ���ʽ �� ��
D������ķ���ʽC2H4O2
�ο��𰸣�D
���������A�в��DZ��ķ���ʽ���ṹ��ʽΪ ���ṹ��ʽӦ���ֳ������ţ�������ϩ�Ľṹ��ʽΪCH2��CH2��B����ȷ�����Ȼ�̼������ÿ����ԭ�ӻ�ԭ3�Ե��Ӳ�����ɼ������Ե���ʽΪ ���ṹ��ʽӦ���ֳ������ţ�������ϩ�Ľṹ��ʽΪCH2��CH2��B����ȷ�����Ȼ�̼������ÿ����ԭ�ӻ�ԭ3�Ե��Ӳ�����ɼ������Ե���ʽΪ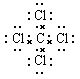 ��������ȷ�Ĵ���D�� ��������ȷ�Ĵ���D��
�����Ѷȣ�һ��
3��ѡ���� ����һ��ת���У�һ��Ҫ��������������ʵ�ֵ��ǣ�?��
A��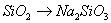
B��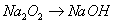
C��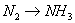
D��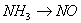
�ο��𰸣�D
����������������ڷ�Ӧ�еõ����ӣ��й�Ԫ�صĻ��ϼ۽��͡���˵��ѡ���е���Ӧ����ʧȥ���ӣ����ϼ����ߣ��ݴ˿�֪ѡ��D�е�Ԫ�صĻ��ϼ����ߣ���Ҫ������������A�л��ϼ۲��䣬����Ҫ��������B�й�����������ˮ����������������ԭ��Ӧ���ɣ�C�е�Ԫ�صĻ��ϼ۽��ͣ���Ҫ���뻹ԭ������ѡD��
�����������Ǹ߿��еij������ͺͿ��㣬�����е��Ѷȵ����⡣���������ǿ��ע������ԣ�ּ�ڿ���ѧ���������������ԭ��Ӧ���й�֪ʶ���ʵ�����������������������ѧ��������������������Ĺؼ���Ҫע����������������ԭ��Ӧ�����ʡ�
�����Ѷȣ�һ��
4������� �ƽ�����ʢ��ǿ��ԭ���£�N2H4����ǿ������Һ̬˫��ˮ�������ǻ�Ϸ�Ӧʱ������������������ˮ���������ų������ȡ���֪0.4molҺ̬��������Һ̬˫��ˮ��Ӧ�����ɵ�����ˮ�������ų�256.652KJ��������
��1��д����������ĵ���ʽ?��
��2���÷�Ӧ���Ȼ�ѧ����ʽΪ?��
1mol����ȫ��Ӧת�Ƶ�����?��
��3���˷�Ӧ���ڻ���ƽ������ͷŴ����ȺͿ��ٲ������������⣬����һ���ܴ���ŵ���?��
��4������֪H2O(l)==H2O(g)����H = +44kJ?mol-1����16gҺ̬����Һ̬˫��ˮ��Ӧ����Һ̬ˮʱ�ų���������?kJ��
�ο��𰸣���1��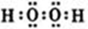 ��2��N2H4��l��+2H2O2��l���TN2��g��+4H2O��g�� ��H=-641.6KJ/mol��4NA ��2��N2H4��l��+2H2O2��l���TN2��g��+4H2O��g�� ��H=-641.6KJ/mol��4NA
��3������������Ⱦ?��4��408.8
�����������1�����������������ԭ������ԭ��֮���γɼ��Լ�����ԭ������ԭ��֮���γɷǼ��Լ�������ʽΪ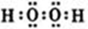 �� ��
��2����֪0.4molҺ̬�º�����˫��ˮ��Ӧ���ɵ�����ˮ����ʱ�ų�256.652KJ���������º�˫��ˮ��Ӧ���Ȼ�ѧ����ʽ��N2H4��l��+2H2O2��l���TN2��g��+4H2O��g�� ��H=-641.6KJ/mol���·����е�Ԫ�صĻ��ϼ��ǣ�2�ۣ���Ӧ���Ϊ0�ۣ�ʧȥ2�����ӣ���1mol����ȫ��Ӧת�Ƶ�����Ϊ4NA��
��3����ԭ���£�N2H4����ǿ������H2O2�������ǻ��ʱ�������������ĵ�����ˮ���������ͷŴ��������Ϳ��ٲ������������⣬���к�ͻ�����ŵ��ǣ�����Ϊ������ˮ������Ⱦ���ʴ�Ϊ������Ϊ������ˮ������Ⱦ��
��4����N2H4��l��+2H2O2��l���TN2��g��+4H2O��g������H=-641.6KJ/mol����H2O��l��=H2O��g������H=+44KJ/mol�����ݸ�˹���ɢ�-�ڡ�4�õ���N2H4��l��+2H2O2��l���TN2��g��+4H2O��L������H=-817.6KJ/mol����ѧ����ʽ��32gȫ����Ӧ����817.6KJ��16gҺ̬��������˫��ˮ��Ӧ���ɵ�����Һ̬ˮʱ���ų���������408.8KJ��
�����Ѷȣ�һ��
5�������� ��10�֣������£���20g�����������Һ�У���μ���17.1%������������Һ������Һ�μ���20gʱ�����ᱵ�����ﵽ����ֵ������Һ�μ���60gʱ����ҺpH����7����
��1����ʼ���Һ�����������������
��2����ʼ���Һ��HCl������������
��3��25��ʱ������ҺpH=7ʱ����������Һ�е�ˮ43.02g����ȴ��ԭ�¶Ⱥ��˺�ɵ�4.98g���塣���ʱ�Ȼ������ܽ�ȡ�
�ο��𰸣���1�������ᷴӦ������������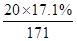 =0.02mol =0.02mol
��ԭ��������������������Ϊ�� ��100%=9.8% ��100%=9.8%
��2�������ᷴӦ������������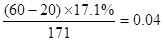 mol mol
��ԭ�������HCl%��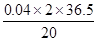 ��100% = 14.6% ��100% = 14.6%
��3�����������ᱵ��������0.02��233 = 4.66g��
�����Ȼ�����0.04��208=8.32g����Ϊ4.98>4.66��������Ҳ���Ȼ����������������µ���ҺΪ�Ȼ����ı�����Һ�������Ȼ���������4.98-4.66=0.32g��
�����Ȼ�����Һ�������Ȼ���������Ϊ��8.32-0.32=8.00g
������Һ����������20+60��-��43.02+4.98��=32.00g
�Ȼ������ܽ�ȣ�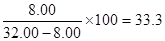 g g
�������������pH�������������ܽ�ȵ��йؼ��㡣
�����Ѷȣ�һ��
|