1、选择题 下列物质不能导电,但属于电解质的是
A.NaCl晶体
B.铜
C.盐酸溶液
D.蔗糖
参考答案:A
本题解析:略
本题难度:一般
2、填空题 明矾溶于水会产生胶状Al(OH)3,Al(OH)3是一种弱电解质,它的碱式电离方程式为:______;
Al(OH)3有很强的吸附能力,能吸附水里的杂质,所以明矾可用作______剂.
参考答案:Al(OH)3是一种弱电解质,在水中部分电离,其电离方程式为:Al(OH)3?Al3++3OH-;明矾溶于水会产生胶状的Al(OH)3有很强的吸附能力,能吸附水里的杂质,所以明矾可用作净水剂.
故答案为:Al(OH)3?Al3++3OH-;净水.
本题解析:
本题难度:简单
3、填空题 某二元酸(化学式用H2A表示)在水中的电离方程式是:
H2A = H+ + HA- HA- H+ + A2-
H+ + A2-
回答下列问题:
?(1)用离子方程式表示Na2A溶液显"酸性""或中性"或"碱性"的原因 __________________________________________
(2)在0.1mol.L-1的Na2A溶液中,下列微粒浓度关系式正确的是__________
A.c(A2-) +c( HA-)+c( H2A) =0.1mol・L-1
B.c(OH-)=c(H+) +c( HA-)+2c(H2A)
C.c(Na+)+ c(H+) =c(OH-)+ c( HA-)+2c(A2-)
D.c(Na+ ) >c(A2-)>c( HA-) >c(OH-) >c(H+)
(3)常温下,已知0.1mol・L-1NaHA溶液的pH=2,则当H2A溶液中c(H+)为0.11 mol・L-1时,H2A溶液的物质的量浓度应___________ 0.1mol/L(填">"或"<"或"="); 理由是_______________________________。
(4)比较①0.1mol・L-1 Na2A溶液 ②0.1mol・L-1 Na2SO4溶液,两种溶液中阴离子总浓度的大小①_________ ②(填">"或"<"或"=")。
参考答案:(1)A2- + H2O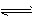 HA- + OH-
HA- + OH-
(2)ABC?
(3)> ;H2A-级电离出H+ ,对HA-电离起抑制作用,而NaHA中不存在抑制
(4)>
本题解析:
本题难度:困难
4、选择题 关于电解质强弱及非电解质的组合完全正确的是
[? ]
?
强电解质?
弱电解质?
非电解质?
A.
NaCl
HF
Cl2
B.
H2SO4
BaSO4
CS2
C.
CaCO3
HClO
C2H5OH
D.
HNO3
CH3COOH
SO2
参考答案:CD
本题解析:
本题难度:简单
5、选择题 下列叙述正确的是
[? ]
A.NaCl溶液在电流作用下电离成Na+和Cl-
B.NaCl是电解质故NaCl晶体能导电
C.氯化氢溶于水能导电,但液态氯化氢不能导电
D.导电性强的溶液里自由移动离子数目一定比导电性弱的溶液里自由移动离子数目多
参考答案:C
本题解析:
本题难度:简单