1��ѡ���� ʵ����������950mL? 0.1 mol��L������ͭ��Һʱ�����в�����ȷ����
A����ȡ15.2g����ͭ���壬����1000 mLˮ
B����ȡ2 4g��������ˮ���1000 mL��Һ
4g��������ˮ���1000 mL��Һ
C����ȡ16 g����ͭ���壬����1000 mLˮ
D����ȡ25 g��������ˮ���1000 mL��Һ
�ο��𰸣�D
�����������
�����Ѷȣ�һ��
2������� ��д�������йط�Ӧ�Ļ�ѧ����ʽ��
��1��ʪ����ͭ������������ͭ��Һ��Ӧ:?
(2)�������������ڸ����·������ȷ�Ӧ��?
��3��������ڵ��Ȼ�þ�ƽ���þ��?
��4���Ҵ�������Ʒ�Ӧ��?
�ο��𰸣���1��Fe��CuSO4=Cu��FeSO4?(2)Fe2O3��2Al Al2O3��2Fe
Al2O3��2Fe
(3)MgCl2�����ڣ�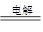 Mg��Cl2��?��4��2CH3CH2OH��2Na
Mg��Cl2��?��4��2CH3CH2OH��2Na 2CH3CH2ONa��H2��
2CH3CH2ONa��H2��
���������
��1��Fe��CuSO4=Cu��FeSO4?(2)Fe2O3��2Al Al2O3��2Fe
Al2O3��2Fe
(3)MgCl2�����ڣ�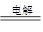 Mg��Cl2��?��4��2CH3CH2OH��2Na
Mg��Cl2��?��4��2CH3CH2OH��2Na 2CH3CH2ONa��H2��
2CH3CH2ONa��H2��
���������ұ�������ʵķ���ʽ��д��ע��������غ㣬��Ҫ��ƽ�ڵ����غ㣬������ԭ��Ӧ��ʧ������ͬ�۷�Ӧ������ȫ������ȷ��
�����Ѷȣ���
3��ѡ���� FeCl3��CuCl2�Ļ����Һ�м������ۣ���ַ�Ӧ�����й�����ڣ������жϲ���ȷ����
[? ]
A.����KSCN��Һһ�������ɫ
B.��Һ��һ������Fe2+
C.��Һ��һ����Cu2+
D.ʣ�������һ����ͭ
�ο��𰸣�C
���������
�����Ѷȣ���
4��ѡ���� ��пƬ����Ƭ����ʢ��ʳ��ˮ�ͷ�̪�ı������У���ͼ��ʾ��
���ȹ۲쵽��̪���������������

A��I��III
B��I��IV
C��II��III
D��II��IV
�ο��𰸣�B
���������
��ȷ�𰸣�B
���ԭ��أ�I��������2H2O��2e-=H2��2OH�D��������ǿ���ұߵ��أ� IV��������2H2O��2e-=H2��2OH�D��������ǿ
�����Ѷȣ���
5������� ͭ�����������Ԫ�أ�Ҳ����������ʹ�õĽ���֮һ��ͭ��������ʹ�öԹ����������������������Զ��Ӱ�졣�����(1)��(3)�⣺
(1)�������ż������м��أ����������Ϊͭ[������(CuSO4)������Ӧ����ͭ]����д���÷�Ӧ�Ļ�ѧ����ʽ�� _____________________________��
(2)ͭ��������ʱ������ͭ�̣���д������ͭ�̵Ļ�ѧ����ʽ��____________________________��
���ͭ�̿����û�ѧ������ȥ����д����ȥͭ�̶�����������Ļ�ѧ����ʽ�� _________________________��
(3)ͭǮ����ʷ��������һ�ֹ㷺��ͨ�Ļ��ҡ��Դ��������ʺͻ�ѧ���ʵĽǶȷ���Ϊʲôͭ������������ҡ�(ͭ���۵���1 183.4 �棬�����۵���1 534.8 ��)_________________ ___________��
�ο��𰸣�(1)Fe��CuSO4=FeSO4��Cu
(2)2Cu��O2��H2O��CO2=Cu2(OH)2CO3
Cu2(OH)2CO3��4HCl=2CuCl2��CO2����3H2O
(3)ѡ��ͭ����������Ϊͭ���۵�Ƚϵͣ�����������ͣ�ͭ�Ļ�ѧ���ʱȽ��ȶ������ױ���ʴ
������������⿼���й�ͭ��ұ��������ͭ����������ʣ�ͬʱ�������й�ͭ��
Ӧ�á�һ����Ҫע��ͭ�����ʺ��ȶ�����������ѧ��Ӧ������Ӧ֪������
�ȶ�������Եģ�������������Ҳ����һЩ���ʷ�Ӧ��
�����Ѷȣ�һ��